Антибиотикотерапия при кишечной непроходимости
Оглавление темы “Тонкокишечная непроходимость.”:
1. Ведение больного с тонкокишечной непроходимостью. Жидкостно-электролитный баланс. Назогастральное дренирование.
2. Когда оперировать больного с тонкокишечной непроходимостью? Пассаж гастрографина.
3. Дополнительные исследования при тонкокишечной непроходимости. Антибиотики при тонкокишечной непроходимости.
4. Операция при тонкокишечной непроходимости. Техника операции при тонкокишечной непроходимости.
5. Проводить ли декомпрессию кишечника при тонкокишечной непроходимости?
6. Девственный живот. Пациент с заранее известным онкологическим заболеванием.
7. Радиационный энтерит. Многократно рецидивирующая тонкокишечная непроходимость.
8. Желчнокаменная непроходимость. Прогноз тонкокишечной непроходимости.
9. Ущемленные грыжи брюшной стенки. Клиническая картина ущемления грыжи.
10. Подготовка к операции при ущемленной грыже брюшной стенки. Операция при паховой грыже.
Дополнительные исследования при тонкокишечной непроходимости. Антибиотики при тонкокишечной непроходимости.
Данных клинического обследования в сочетании с абдоминальными рентгенограммами, усиленными пассажем гастрографина, достаточно, чтобы в большинстве случаев принять правильное решение. Необходимы ли дополнительные исследования и какие? Некоторым энтузиастам, по их признанию, УЗИ помогло уточнить место обструкции и факт странгуляции вообще.
Однако это должна быть оценка хорошо ориентирующегося специалиста, каковых нет в большинстве лечебных учреждений. КТ, усиленная пероральным или внутривенным контрастированием, также способна уточнить уровень обструкции и распознать сегмент кишки, подвергшийся странгуляции. Но это не означает, что КТ обычно необходима. Она целесообразна в следующих ситуациях:
• В анамнезе онкологическое заболевание; КТ может выявить диффузный канцероматоз с наличием асцита или без него. Возможности лечения в этом случае ограничиваются лишь симптоматической терапией.
• Клиническая картина не соответствует частичной спаечной тонкокишечной непроходимости; в частности, паралитический илеус легко может быть принят за частичную непроходимость: в толстой кишке содержится газ, гастрографин продвигается по кишечнику, но клиническая симптоматика, повышенные температура и лейкоцитоз остаются.
Здесь КТ может документально подтвердить скрытую причину перитонита, поддерживающего паралитический илеус (например, выявить аппендикулярный или дивертикулярный инфильтрат).
Антибиотики при тонкокишечной непроходимости.
В экспериментах с тонкокишечной непроходимостью на животных антибиотики снижают количество кишечных осложнений и уменьшают летальность. В клинических ситуациях необходимости в антибиотиках у пациентов, получающих консервативное лечение, нет.
Мы же оперируем, как только возникает подозрение на угрозу жизнеспособности кишечника. Поэтому достаточно однократного введения антибиотика с профилактической целью перед операцией; в послеоперационном периоде необходимости в продолжении антибактериальной терапии нет, даже если произведена резекция кишки.
Показаниями для антибактериальной терапии в послеоперационном периоде являются длительная предшествующая гангрена тонкой кишки и длительное внутрибрюшинное инфицирование.
– Также рекомендуем “Операция при тонкокишечной непроходимости. Техника операции при тонкокишечной непроходимости.”
Источник

Непроходимость кишечника – это комплекс симптомов, развивающихся на фоне полного или частичного нарушения продвижения пищи по кишечнику. Непроходимость кишечника является грозным состоянием, которое при отсутствии лечения неизбежно осложняется перитонитом, некрозом кишки и приводит к гибели пациента. Поэтому начать лечить такое заболевание нужно как можно раньше.
Причины и виды острой кишечной непроходимости
В зависимости от того, что послужило причиной ее развития, выделяют:
- Динамическую, или функциональную непроходимость. Она развивается из-за нарушения перистальтики кишечника – его спазма или паралича.
- Механическую непроходимость кишечника. Она развивается из-за закрытия просвета кишки и невозможности транзита его содержимого. Здесь различают:
- Странгуляционную непроходимость кишечника, от латинского strangulatio – удушение. Она развивается из-за сдавления кишки или ее брыжейки, в результате которого нарушается кровоснабжение кишечника. Это очень опасное состояние, поскольку может привести к некрозу кишечной стенки.
- Обтурационная непроходимость кишечника. Развивается из-за закупорки (обтурации) просвета кишки инородными телами (конкременты, паразиты), опухолью или рубцовой деформацией.
По месту развития выделяют толстокишечную и тонкокишечную непроходимость.
В онкологии непроходимость кишечника чаще всего носит обтурационный характер и развивается, как осложнение колоректального рака, когда опухоль перекрывает просвет толстой кишки, как правило, в его терминальных стадиях. Обтурация может развиться и в результате сдавления кишки опухолью другого органа, например, матки или предстательной железы.
Непроходимость тонкого кишечника возникает реже. Как правило, ее причиной является канцероматоз висцеральной брюшины. Первичные опухоли в этом отделе встречаются крайне редко.
Последствия непроходимости кишечника
Развитие непроходимости запускает каскад патологических процессов, которые действуют на организм системно. При опухолевой обтурации начало, как правило, носит стертый характер из-за неполной окклюзии просвета кишки, но по мере роста опухоли, ситуация усугубляется. Острая непроходимость, как правило, развивается из-за полной обтурации плотными каловыми массами на суженном опухолью участке кишки.
В первое время после развития непроходимости, отмечается усиление перистальтики кишки. Он как бы хочет преодолеть препятствие. По мере того, как скапливается кишечное содержимое, стенка кишки перерастягивается, возникают водно-электролитные и метаболические нарушения, моторная функция резко ослабевает, а затем и вовсе наступает паралич кишечника.
На втором этапе развиваются нарушения секреторно-резорбтивной деятельности кишечника и нарушения пристеночного пищеварения, блокируется ферментативная активность энтероцитов, поскольку они отторгаются, а регенеративная активность крипт сначала угнетается, а затем и вовсе прекращается.
В таких условиях активируется деятельность кишечных бактерий, и так называемого симбионтного пищеварения. Оно не физиологично и по эффективности уступает нормальному, пристеночному пищеварению. В результате происходит гниение и брожение, а также накопление большого количества продуктов неполного расщепления белков, часть из которых оказывает токсическое действие.
По мере прогрессирования процесса происходит нарушение иммунных механизмов защиты, что приводит к активному размножению анаэробных бактерий, выделяющих экзо- и эндотоксины. Они действуют на организм системно – нарушают микроциркуляцию тканей, приводят к расстройству ЦНС, нарушают клеточный метаболизм. Благодаря этим эффектам увеличивается проницаемость кишечной стенки для бактерий, и они могут распространяться в брюшную полость, кровоток и лимфоток, вызывая перитониты и даже сепсис.
Прогрессируют и водно-электролитные нарушения. За счет нарушения работы кишки происходит усиленная фильтрация жидкости, обратно она не всасывается и скапливается в приводящей петле кишечника. В нормальных условиях в сутки в просвет ЖКТ поступает около 10 л жидкости (с учетом пищи, питья, слюны и секретов пищеварительных желез). Около 8-9 литров должно всасываться обратно, но этого не происходит из-за нарушения реабсорбции. Жидкость скапливается в приводящем отделе кишки, вызывая его расширение. Это, в свою очередь, приводит к рефлекторной рвоте, что еще больше усугубляет обезвоживание. На этом фоне быстро развиваются электролитные нарушения, которые в конечном итоге приводят к почечной и сердечной недостаточности.
Симптомы кишечной непроходимости
- Боли. Это один из самых первых признаков непроходимости кишечника. Он отмечается абсолютно у всех больных. При опухолевой непроходимости боль возникает внезапно, без видимых причин, и может даже являться одним из первых признаков рака. Она имеет схваткообразный характер. Наибольшая болезненность приходится на момент перистальтических сокращений, после чего она немного утихает на пару минут. Постепенно интенсивность болевых ощущений усиливается и через несколько часов они уже носят нестерпимый характер. Стихают они только на 2-3 сутки, когда уже развивается паралич кишки – «шум в начале, тишина в конце», симптом «могильной тишины», когда вообще нет звуков перистальтики.
- Рвота. Если непроходимость располагается на уровне тонкой кишки или правого отдела толстого кишечника, рвота будет присутствовать на ранних стадиях, как признак рефлекторного раздражения ЖКТ. При непроходимости терминальных отделов, рвоты сначала скорее всего не будет или она будет с большими промежутками. В перерывах больные могут страдать от тошноты, икоты или отрыжки. Если непроходимость кишечника сохраняется, рвота приобретает неукротимый характер, сначала выходит застойное содержимое желудка, а потом и кишечника, вплоть до рвоты каловыми массами. Это плохой признак, поскольку он говорит о том, что рвота является симптомом токсического отека головного мозга, и устранить ее с помощью дренирования ЖКТ невозможно.
- Задержка стула. Этот симптом наблюдается при непроходимости на уровне сигмовидной и прямой кишки. При высокой непроходимости в первое время стул может сохраняться.
- Вздутие живота. Здесь выделяют 4 признака: асимметрия живота, пальпируемая выпуклость кишечника, перистальтические сокращения кишечника, которые можно видеть невооруженным глазом, тимпанический звук при перкуссии.
- Кровянистые или слизистые выделения из прямой кишки. Обычно они возникают при раке терминальных отделов кишечника и связаны с секрецией слизи опухолью, ее распадом или травмированием каловыми массами.
В процессе развертывания клинической картины непроходимости кишечника выделяют три периода:
- Ранний – до 12 часов. Основным симптомом этого периода является схваткообразные опухоли в животе. Рвота развивается редко и только при обтурации (закупорке) на уровне тонкого кишечника.
- Промежуточный период – от 12 часов до суток. В это время симптоматика продолжает нарастать и превращается в развернутую картину. Боль становится интенсивной и даже нестерпимой, без схваток, отмечается увеличение живота, рвота, возникают признаки дегидратации.
- Поздний период – более 24 часов. Состояние больного ухудшается, повышается температура, развивается системный воспалительный ответ, вплоть до перитонита и сепсиса. Нарастает отдышка и сердечная недостаточность.
Диагностика кишечной непроходимости
Заподозрить диагноз кишечная непроходимость можно на основании характерных жалоб пациента. Подтверждение производится с помощью инструметального обследования.
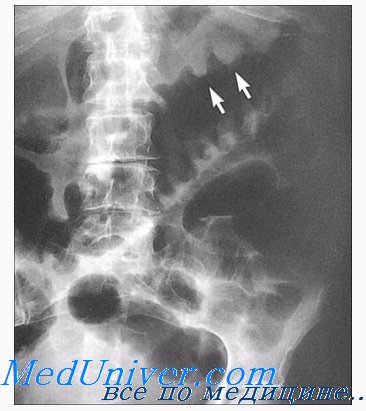
Наиболее простой, быстрый и доступный метод диагностики – это обзорная рентгенография органов брюшной полости. На снимках обнаруживаются характерные признаки:
- Чаша Клойбера – видны расширенные петли кишечника в виде куполов, и в них горизонтальный уровень жидкости. Эта картина напоминает перевернутую вверх дном чашу. Чаш может быть несколько, на снимке они наслаиваются друг на друга.
- Кишечные аркады – возникают из-за раздувания газами петель тонкой кишки, в нижних коленах кишки визуализируется горизонтальный уровень жидкости.
- Складки Керкинга – из-за растяжения тощей кишки на рентгенограммах она приобретает вид растянутой пружины.
- Могут также применяться рентгенологические исследования с контрастированием, например, исследование пассажа бариевой взвеси по ЖКТ, или ирригоскопия. Однако данные методы занимают много времени и затягивают принятие решения о необходимости операции.
Из других методов диагностики применяются:
- Эндоскопическое обследование, например, колоноскопия или ректороманоскопия. Такое исследование помогает определить локализацию новообразования и уровень стеноза в обтурированном сегменте кишечника. В ряде случаев через стенозированный участок удается провести зонд и дренировать приводящий отдел кишки. Колоноскопия не проводится при тяжелом состоянии пациента, наличии симптомов перитонита и угрозе перфорации опухоли.
- КТ. С помощью этого исследования удается визуализировать опухоль, ее размеры и протяженность стеноза (сужения). Кроме того, можно оценить взаимоотношение рака с окружающими тканями и определить наличие метастазов.
- УЗИ. При непроходимости визуализируется увеличение просвета кишечника, скопление в нем воздуха (газов), утолщение стенки кишки за счет воспаления. При развитии системных воспалительных процессов может обнаруживаться свободная жидкость в брюшной полости.
Лечение кишечной непроходимости и первая помощь
Если у пациента подозревают непроходимость кишечника, его немедленно госпитализируют в стационар, поскольку сроки начала лечения напрямую сказываются на прогнозе. Применяются как консервативные, так и хирургические методы.
В рамках консервативной терапии применяются следующие процедуры:
- Декомпрессия кишки. С этой целью может применяться удаление кишечного содержимого выше места обструкции с помощью зондовой аспирации или постановке клизм.
- Коррекция водно-электролитных нарушений, восполнение потери жидкости. С этой целью назначаются инфузии кристаллоидных растворов.
- Купирование боли. Назначаются спазмолитики и анальгетики, например, атропин, платифиллин и др.
- Восполнение потери белка – инфузия белковых препаратов.
- Для профилактики инфекционных осложнений назначаются антибиотики широкого спектра действия.
- Стентирование просвета кишки. С помощью эндоскопа в место непроходимости кишки вводится саморасширяющийся стент. Он раздвигает опухолевые ткани и поддерживает кишку в расправленном состоянии, обеспечивая свободный пассаж ее содержимого. Таким образом, выигрывается время на более тщательную подготовку к плановому вмешательству.
Для онкологических пациентов это особенно актуально, поскольку обширное опухолевое поражение приводит к необходимости наложения колостомы. Установка стента при опухолевой непроходимости дает время для проведения неоадъювантной или периоперационной химиотерапии. Это позволит уменьшить объем опухолевой массы и, возможно, даже провести радикальную операцию. В других случаях это дает шанс наложить обходные анастомозы. Для пациентов в терминальной стадии колоректального рака, у которых есть высокие риски осложнения хирургического вмешательства и наркоза, стентирование является основным методом лечения непроходимости кишечника. После проведения процедуры, пациента продолжают наблюдать и к хирургическому лечению прибегают только в случае развития жизнеугрожающих осложнений.
Во всех остальных случаях показана операция, поскольку опухоль будет продолжать расти и рано или поздно возникнет рецидив непроходимости.
При компенсированном состоянии хирургическое вмешательство может быть отложено на срок до 10 дней, при субкомпенсированном его проводят как можно раньше, после стабилизации с больного. А если есть симптомы перитонита, выполняется экстренная операция.
В любом случае, во время хирургического вмешательства по поводу непроходимости кишечника проводят вскрытие брюшной полости (лапаротомию) с ее ревизией. Определяют расположение опухоли, ее взаимоотношение с окружающими тканями, наличие видимых метастазов. Также выполняют оценку жизнеспособности кишечной стенки с целью определения объема резекции.
В идеале выполняется радикальное удаление опухоли посредством резекции пораженного отдела кишки и восстановление непрерывности кишечника посредством наложения анастомоза. К сожалению, при развитии непроходимости на фоне злокачественного процесса, такой объем операции одноэтапно произвести очень сложно и рискованно, поскольку имеются обширные опухолевые поражения.
Как правило, в таких случаях проводятся паллиативные операции:
- Наложение обходного анастомоза вокруг фрагмента кишки с опухолью. Тем самым непроходимый (обтурированный) отдел исключается из пищеварительной цепи.
- Выведение стомы – отдел кишечника, расположенный выше места непроходимости, выводится на переднюю брюшную стенку в виде отверстия. Через него кишечное содержимое будет отводиться в специальный мешок – калоприемник.
Стомирование является калечащей операцией и тяжело переносится пациентами в моральном плане. Но в этой ситуации на первое место выходит спасение жизни пациента. По возможности, после стабилизации его состояния и устранения последствий кишечной непроходимости проводят дальнейшее лечение, например, химиотерапию, лучевую терапию, и при удовлетворительных результатах проводят реконструктивные вмешательства для восстановления целостности кишки.
Источник
А.А. Зорькин
Кафедра факультетской хирургии с курсом хирургии ФУВ имени проф. И. И. Неймарка
Алтайский государственный медицинский университет (Барнаул)
Инфекционные осложнения в хирургии и интенсивной терапии занимают существенное место среди причин летальности и повышения стоимости оказания медицинской помощи при различной патологии (6, 12). В том числе это касается оперативных вмешательств на толстой кишке, особенно проводимых на фоне преклонного возраста, тяжелой сопутствующей патологии или развившихся осложнений онкопроцесса. Кишечная микрофлора является одним из важных факторов риска развития этих осложнений.
Так, в 20-е годы прошлого века, смертность, обусловленная гнойно-септическими осложнениями, после резекций толстой кишки по поводу ее опухоли, превышала 43%. Использование достижений хирургии, анестезиологии и интенсивной терапии позволило снизить этот показатель до 2,6-14%. При этом общее количество гнойно-септических осложнений при проведении плановых резекций, по сведениям Американского общества колоректальных хирургов, может составлять от 6 до 25%. Нагноения ран составляют более 20%, формирование забрюшинных инфильтратов и абсцессов – до 8%, формирование абсцессов и инфильтратов брюшной полости, послеоперационный перитонит – около 4% (13, 17). С. В. Сидоренко и С. В. Яковлев приводят данные о частоте осложнений при вмешательствах на толстом кишечнике в пределах 15-30% (данные мета-анализа 147 клинических исследований – 11%), при наличии перитонита эти осложнения наблюдаются в 20- 40% случаев (11).
Среди механизмов инфицирования большое значение имеют не только общепризнанные факторы, имеющиеся при любых инвазивных вмешательствах (качество обработки операционного поля, рук медперсонала, инструментария и белья и т.д.). Существенным является качество подготовки толстой кишки, наличие инфекционных (перитонит, перифокальное воспаление) или неинфекционных (толстокишечная непроходимость, кровотечение, анемия) осложнений основного заболевания (4, 5). Эти факторы часто встречаются в неотложной колоректальной хирургии. Большинством исследователей признается прямая зависимость между частотой нагноений и бактериальной обсемененностью операционного поля (6, 7, 10, 14). Кроме того, около 65% операций на толстой кишке заканчивается наложением колостомы (13), что в раннем послеоперационном периоде может привести к аутоинфицированию послеоперационной раны.
Исследования продемонстрировали относительную лабильность состава толстокишечной микрофлоры. Так, соотношение облигатных анаэробов и аэробов колеблется от 100:1 до 1000:1. В норме в 1 грамме фекалий постоянно присутствуют бифидобактерии (108 – 109 микробных тел), бактероиды (109 – 1010), лактобациллы (106 – 107), молочнокислый стрептококк (106 – 108), спорообразующие клостридии (105), лактозоферментирующая кишечная палочка (107 – 108), энтерококки (105 – 106), дрожжеподобные грибы, коагулазонегативные стафилококки (по 104). Не всегда выделяются лактозодефицитная и лактозонеферментирующая кишечная палочка (105 – 107), гемолизирующая кишечная палочка (106), протей (104), клебсиелла и другие грамотрицательные условные патогены (по 105), S. aureus (103) и плесневые грибы (104). При исследовании колонобиоптатов показано, что характер и количество микроорганизмов в слизистой толстой кишки существенно отличается от таковых в ее просвете. Постоянно выделяются лактозодефицитная, лактозонеферментирующая и гемолизирующая кишечная палочка (по 104), лактобациллы, протей и клебсиелла (по 102), другие грамотрицательные условные патогены (по 101), S. aureus и плесневые грибы (менее 101). Не во всех случаях встречаются бифидобактерии, бактероиды, стрептококки и коагулазонегативные стафилококки, лактозоферментирующая E. coli, энтерококки и дрожжеподобные грибы (13). Поэтому при плановых вмешательствах на толстой кишке риск развития несостоятельности швов анастомозов и гнойно – септических осложнений, прежде всего интраабдоминальных абсцессов, ниже, чем при операциях на неподготовленном кишечнике или в условиях острой кишечной непроходимости.
Патологические процессы, возникающие при развитии некоторых осложнений, способствуют изменению характера микрофлоры как толстой, так и тонкой кишки. Показано, что при острой кишечной непроходимости с явлениями перитонита достоверно увеличивается число как аэробов, так и анаэробов в просвете тонкой кишки, приближаясь к среднему числу бактерий, содержащихся в толстой кишке, утрачивается их нормальный градиент от тощей к подвздошной кишке (5). В настоящее время у больных с тяжелой хирургической патологией признан значимым транслокационный механизм развития полиорганной недостаточности (15), что подразумевает “прорыв” кишечного барьера с развитием не только портальной и системной бактериемии, но и инфицированием перитонеальной жидкости, развитием вторичного распространенного перитонита без перфорации стенки кишки. Все это требует формирования серьезного подхода к тактике антибактериальной терапии в колоректальной хирургии как при плановых, так и при экстренных вмешательствах. Вполне логичным в этой связи выглядит назначение антибактериальных препаратов с целью подавления активности кишечной флоры.
Исторически метод стерилизации кишечника перед операцией возник в 30-е годы прошлого века как профилактическая мера при операциях на толстой кишке. Для этих целей применяли большие дозы сульфаниламидов, назначаемые per os. В дальнейшем предпочтение отдавалось пероральному назначению аминогликозидов (канамицин, гентамицин), которое в плацебо – контролируемых исследованиях дало снижение частоты раневой инфекции с 43% до 9% (17). После установления ведущей роли анаэробной микрофлоры в развитии послеоперационных инфекционных осложнений, возрос интерес к препаратам с антианаэробной активностью (клиндамицин, тетрациклин, метронидазол), которые применялись парентерально. В целом, с течением времени предпочтение стало отдаваться методикам системного применения антибиотиков широкого спектра действия, более действенных для профилактики гнойно – септических осложнений. Это снизило частоту раневой инфекции с 30 – 60% до 3 – 9% (10, 16, 17).
Существующие рекомендации по комбинированной профилактике осложнений в колопроктологии очень разнородны (2, 4, 5, 6, 8, 9, 10, 11, 13, 16, 17). Целесообразным является принципиальное их разделение: 1) используемые при плановых ситуациях; 2) используемые в неотложной абдоминальной хирургии.
При плановых оперативных вмешательствах на толстой кишке необходимо использование следующих подходов.
- Тщательная подготовка толстой кишки с использованием механических методов. К ним относятся традиционные способы (назначение бесшлаковых и элементарных диет – стол № 4, вивонекс, ЭНПИТ, нутризон, нутридринк и т.п., применение слабительных – касторовое масло, сульфат магния, вазелиновое масло, клизмы – очистительные, сифонные, по Огневу и методики Fleet – enema). В специализированных центрах и отделениях возможно широкое применение метода ортоградного кишечного лаважа изо – и гиперосмолярными растворами электролитов, маннитола, полиэтиленгликоля, фортрансом (8, 13).
- Системная антибиотикопрофилактика, которая считается “золотым стандартом” профилактики инфекционных осложнений в хирургии. Оперативные вмешательства на толстой кишке являются абсолютным показанием к проведению периоперационной антибиотикопрофилактики. С этой целью рекомендуется использование следующих препаратов: амоксициллин/клавуланат 1,2 г в/в за 30-40 минут до операции, ампициллин/сульбактам 1,5 г в/в за 30-40 минут до операции, цефуроксим 1,5 г в/в за 30-40 минут перед операцией с 0,5 г метронидазола, цефокситин 2,0 г в/в за 30-40 минут до операции (9, 11).
- Локальная антибиотикопрофилактика (пероральная селективная деконтаминация). Проводится в день, предшествующий операции (11) – неомицин 1,0 г + эритромицин 1,0 г + метронидазол 1,0 г; полимиксин + гентамицин + амфотеррицин В (или нистатин). Л. С. Страчунский с соавт. рекомендуют сочетание канамицина 1,0 с эритромицином 1,0 г в 13-00, 14-00, 23-00 в день перед операцией и в 8-00 в день операции (9).
При проведении экстренных вмешательств на толстой кишке более отчетливо проявляется роль антибактериальных средств в профилактике гнойно – септических осложнений (1, 3, 6, 9, 16). Действительно, механическая подготовка кишки и локальная антибиотикопрофилактика у этой категории пациентов не проводится либо из – за короткой продолжительности предоперационного периода (острая кишечная непроходимость, вторичный распространенный перитонит), либо из – за наличия прямых противопоказаний (перфорация кишечника, полиорганная недостаточность).
Необходимо системное назначение антибактериальных препаратов: гентамицин 80 мг + метронидазол 0,5 г или амоксициллин/клавуланат 1,2 г или ампициллин/сульбактам 1,5 г внутривенно за 30 минут перед операцией (9). Альтернативой защищенным пенициллинам является цефалоспорин 2 поколения с антианаэробной активностью – цефокситин, вводимый в дозе 2,0 г в/в за 30 минут до операции. Наличие интраоперационных признаков перитонита или запущенной кишечной непроходимости требует проведения антибактериальной терапии теми же препаратами по общепринятым правилам продолжительностью от 5 до 15 суток.
Большое значение имеет ранняя декомпрессия кишечника при острой кишечной непроходимости, что должно стать обязательным этапом любой операции по поводу этой патологии. Необходимым условием благоприятного течения послеоперационного периода является проведение адекватной периоперационной интенсивной терапии, включая назо-интестинальную интубацию кишечника, фракционный кишечный лаваж, чреззондовую селективную деконтаминацию кишечника и энтеросорбцию (2, 3). У больных с колостомами с целью профилактики послеоперационного инфицирования лапаротомной раны целесообразно раннее, с момента раскрытия просвета кишки, ношение калоприемника, желательно на липкой основе.
Литература
1. Гарау Х. Основы рационального выбора антимикробных препаратов при интраабдоминальных инфекциях. // Клиническая микробиология и антимикробная химиотерапия, 2002, т. 4, № 3, с. 278 – 287.
2. Гельфанд Б. Р., Гологорский В. А., Бурневич С. З. и соавт. Селективная деконтаминация и детоксикация желудочно – кишечного тракта в неотложной абдоминальной хирургии и интенсивной терапии. // Вестник интенсивной терапии, 1995, № 1, с. 8 – 11.
3. Гельфанд Б. Р., Бурневич С. З., Гельфанд Е. Б., Попов Т. В. Антибактериальная терапия интраабдоминальных хирургических инфекций. // Фарматека, 2003, № 1, с. 68 – 73.
4. Даценко Б. М., Пулатов А. К., Дружинин Е. Б. Подготовка толстой кишки к операции при кишечной непроходимости. // Хирургия, 1994, № 10, с. 41 – 44.
5. Ерюхин И. А., Петров В. П., Ханевич М. Д. Кишечная непроходимость. Руководство для врачей. – СПб: Изд – во “Питер”, 1999. – 448 с.
6. Зубков М. Н. Антибактериальная профилактика госпитальных хирургических инфекций. // Фарматека, 2003, № 1, с. 62 – 67.
7. Кныш В. И., Ананьев В. С. Гнойные осложнения после операций по поводу рака толстой кишки. // Хирургия, 1985, № 3, с. 138 – 143.
8. Перов Ю. А., Постолов П. М., Попова И. С. Сравнительная оценка методов подготовки толстой кишки к операции. // Хирургия, 1987, № 1, с. 108 – 115.
9. Практическое руководство по антиинфекционной химиотерапии./ Под ред. Страчунского Л.С., Белоусова Ю.Б., Козлова С.Н. – Москва, 2002. – 381 с.
10. Рациональная антимикробная терапия. Руководство для практикующих врачей / Под ред. В. П. Яковлева, С. В. Яковлева. – М.: Литерра, 2003. – 1008 с.
11. Сидоренко С. В., Яковлев С. В. Инфекции в интенсивной терапии. – М.: Изд – во “Бионика”, 2003. – 208 с.
12. 50 лекций по хирургии / Под ред. В. С. Савельева. – М.: Медиа Медика, 2003. – 408 с.
13. Ханевич М. Д., Шашолин М. А., Зязин А. А. Колоректальный рак: подготовка толстой кишки к операции. – М.: МедЭкспертПресс; Петрозаводск: ИнтелТек, 2003. – 136 с.
14. Dawes L. G., Aprachamian C., Condon R. E., Malangoni M. A. The risk of infection after colon injury. // Surg, 1986, V 100: 796 – 803.
15. Marshall L. F., Camp P. E., Bowers Sh. A. The gastrointestinal tract: the “undraind abscess” of multiple organ failure // Ann. Surg., 1993; Vol. 218, N 1: 111 – 119.
16. Song F., Glenny A. M. Antimicrobial prophylaxis in colorectal surgery: a systematic review of randomized control trials. // Br. J. Surg., 1998; 85: 1232 – 1241.
17. Weaver M., Burdon D. V., Youngs D. J. Oral neomycin and erythromycin compared with singler – dose systemic metronidazole and ceftriaxone prophylaxis in elective colorectal surgery. // Am. J. Surg., 1986; 151: 437 – 442.
Источник: www.abolmed.ru
Источник
