Дисбактериоз носоглотки у ребенка
Слизистая оболочка верхних дыхательных путей представляет собой первую линию защиты организма против разнообразных патогенных факторов окружающей среды, таких как бактериальные, грибковые, вирусные, промышленные химические раздражители и загрязнения и обеспечивает противовирусный иммунитет. Повреждение слизистой или сухость облегчают проникновение вируса в организм. После того, как враг попал в организм и начал повреждать клетки, огромное значение играет выработка интерферонов, которые обеспечивают их невосприимчивость к действию вируса.
Противовирусный иммунитет – это очень сложный процесс, в котором участвует множество ресурсов иммунной системы. К сожалению, иммунные реакции не всегда срабатывают так, как об этом пишут в учебниках по биологии. Часто какой-либо процесс может быть нарушен, что приводит к осложнениям и проблемам. Когда снижен иммунный ответ, нужны средства, поднимающие иммунитет. Они могут быть природными, либо купленными в аптеке, главное – это эффективность и безопасность.
Слизистая оболочка верхних дыхательных путей большей частью покрыта тонким специализированным эпителием, создающим восприимчивый (чувствительный) барьер, который постоянно бомбардируется экзогенным живым или мертвым антигенным материалом.
Вдыхаемый воздух содержит значительное количество потенциально вредных веществ (газы, взвешенные корпускулярные частицы, бактерии, вирусы, микоплазмы, грибы, в том числе дрожжи, риккетсии, пыльцу, частицы слущенного эпителия человека и животных и др.). Согласно концепции местного иммунитета, слизистые оболочки и кожа как покровы, обращенные во внешнюю среду, защищают внутреннюю среду организма и сохраняют постоянство внутренней среды путем тесного взаимодействия эволюционно выработанного комплекса неспецифических и специфических механизмов защиты.
Местный иммунитет ЛОР-органов – это барьерная функция слизистых оболочек, включающая лимфоэпителиальные органы глотки, расположенные на пересечении воздухоносных и пищепроводных путей, первыми реагирующие на очередное антигенное раздражение (инфекцию) включением механизмов иммунной защиты, и неспецифические защитные факторы слизистой оболочки (мукоцилиарный транспорт, продукция лизоцима, лактоферрина, интерферона и др.)
А теперь непосредственно о микрофлоре верхних дыхательных путей и полости рта. Важно понимать, что ЛОР-органы не являются исключением в отношении микробной стерильности, т. е. в норме мы можем выявлять определенные микроорганизмы в носу, глотке и наружном ухе. Эти микробы в условиях сохранения иммунной резистентности не только не приносят нам никакого вреда, но и наоборот, оказывают положительное влияние. Они образуют так называемую биопленку (толщиной от 0,1 до 0,5 мм) – полисахаридный каркас которой, состоящий из микробных полисахаридов и муцина, предотвращает заселение организма патогенными микроорганизмами. Благодаря выделению микроорганизмами биопленки различных кислот, спирта, лизоцима (антибактериальное вещество) и стимуляции образования иммуноглобулина А тормозится развитие патогенных микробов. Кроме того, нормальные микроорганизмы препятствуют выделению токсинов патогенными бактериями.
Иллюстрацией работы «полезных» микроорганизмов является, например, следующий факт: с каждым вдохом мы в среднем вдыхаем около 1400-1700 микробов, а благодаря, в частности, биологическим факторам неспецифической защиты в глотке их количество сокращается до 300, в гортани и нижележащих отделах эти микроорганизмы не обнаруживаются вообще.

Это лишний раз подтверждает важность сбалансированной микрофлоры для полноценной жизнедеятельности всего организма.
Нормальная микрофлора глотки разнообразна, поскольку здесь смешивается микрофлора полости рта и воздухоносных путей. Представителями резидентной микрофлоры считаются: нейссерии, дифтероиды, и гемолитические стрептококки, энтерококки, микоплазмы, коагулазоотрицательные стафилококки, моракселлы, бактероиды, боррелии, трепонемы, актиномицеты. В верхних дыхательных путях преобладают стрептококки и нейссерии, помимо этого встречаются стафилококки, дифтероиды, гемофильные бактерии, пневмококки, микоплазмы, бактероиды. Слизистая оболочка гортани, трахеи, бронхов в норме стерильна. Следует сказать, что вышеуказанный видовой спектр микроорганизмов не является неизменным. Его состав зависит от многих факторов: сопутствующей патологии, возраста, условий внешней среды, условий труда, питания, перенесенных заболеваний, травм и стрессовых ситуаций и т.д.
Такие состояния, как острые и хронические заболевания всего организма, а особенно уха, горла, носа и полости рта, аллергия, неблагоприятные физические факторы (переохлаждение, инсоляция и т. д.), химические агенты, физическое, интеллектуальное и психоэмоциональное перенапряжение, прием антибактериальных, гормональных и цитостатических препаратов, недостаточное питание, гиповитаминоз, профессиональные вредности, курение, алкоголь провоцируют нарушение нормального микробиологического равновесия в ЛОР-органах и являются причинами нарушения качественного и количественного состава микрофлоры ротоглотки. Существует бактериологическое понятие, которое характеризует изменение соотношения представителей нормальной микрофлоры, снижение числа или исчезновение некоторых видов микроорганизмов за счет увеличения количества других и появления микробов – это дисбактериоз.
Терапия дисбактериоза должна быть строго индивидуальной и направленной в первую очередь на ликвидацию источника проблемы. Например, пока не будет адекватно пролечен аденоидит (консервативно или оперативно), от дисбактериоза вряд ли возможно избавиться. Вопрос о необходимости приема антибиотика определяется исключительно течением основного заболевания: если дисбактериоз глотки вызван наличием у ребенка хронического панкреатита, то антибактериальные средства тут неуместны; если же дисбактериоз связан с запущенной формой хронического синусита или аденоидита – без этой группы лекарственных препаратов, скорее всего, не обойтись. Воспалительные очаги в носо- и ротоглотке должны быть обязательно устранены – кариозные зубы пролечены, аденоидные вегетации, небные миндалины санированы и т.д. Помните, что они могут не только вызывать местные воспалительно-инфекционные процессы и дисбактериоз ротоглотки, но и являться источником аутоинфекции и аутоинтоксикации всего организма. Убедительные данные свидетельствуют, что возникновение ряда заболеваний респираторной, желудочно-кишечной, сердечно-сосудистой систем, опорно-двигательного аппарата обусловлено очаговой инфекцией в ротоглотке. Поэтому санация полости рта и ЛОР-органов – это обязательное условие и первый шаг к выздоровлению при многих патологических процессах.
Не стоит также забывать о мерах профилактики развития инфекционно-воспалительных процессов ротоглотки и ЛОР-органов. Так, стандартными мерами профилактики являются: ежедневные гигиенические мероприятия (туалет носа), регулярное посещение врача, рациональное питание, закаливание, создание оптимального микроклимата (влажность, температура), лечение сопутствующей патологии.
Кроме вышеперечисленных мер профилактики, помочь решить проблему инфекционно-воспалительных заболеваний ЛОР-органов и помочь восстановить нормальный микробиоценоз слизистой оболочки может прием средств растительного происхождения на основе прополиса.
Прополис – это смесь природных смол, вырабатываемых пчёлами из соединений, собираемых с разных частей растений, бутонов и выделений. Современные противомикробные применения прополиса включают рецептуры для лечения синдрома простуды (инфекции верхних дыхательных путей, обычная простуда и гриппоподобные инфекции), для заживления ран, лечения ожогов, акне, простого и генитального герпеса, и нейродермита.
В настоящее время, прополис является природным лечебным средством, он применяется и в косметике и является популярным альтернативным лекарственным средством для самолечения различных заболеваний. Современное применение прополиса предполагает его использование для лечения синдрома простуды (инфекции верхних дыхательных путей, обычная простуда и гриппоподобные инфекции), а также в качестве дерматологических препаратов, полезных для заживления ран, лечения ожогов, акне, простого и генитального герпеса, и нейродермита. Прополис также применяют для полоскания рта для предупреждения кариеса и для лечения гингивита и стоматита. На рынке он представлен в комбинации с экстрактом тимьяна, меда и витамина С в форме спрея для полости рта и горла Санорин Лорис, который не содержит спирта и является водно-глицериновым раствором. Благодаря комбинации натуральных компонентов и их свойствам, спрей Санорин Лорис эффективен для гигиены полости рта и для профилактики раздражения, увлажнения и защиты слизистой горла, а также как дополнение к комплексному лечению и профилактике ОРЗ. Важно отметить, что это удобный спрей для использования в любой ситуации, достаточно встряхнуть флакон и направить распылитель на проблемный участок.
Источник
Комментарии
Опубликовано в журнале:
Вопросы современной педиатрии /2014/ Том 13/ № 1
Д.А. Тулупов, Е.П. Карпова
Российская медицинская академия последипломного образования, Москва, Российская Федерация Представлен обзор результатов клинических исследований по изучению роли патогенной бактериальной флоры в этиологии хронического аденоидита у детей. Согласно литературным данным, основной причиной развития хронической патологии носоглотки у детей является вирусная инфекция. При этом роль бактериальной микрофлоры в развитии хронического аденоидита вторична, но весьма существенна. Основными бактериальными патогенами, выделяемыми из носоглотки детей с хроническим аденоидитом, являются Staphylococcus aureus, Haemophilus influenzae и Streptococcus pneumoniae, однако существует выраженная диссоциация в частоте выделения данных бактериальных патогенов по данным разных исследователей. Значительную роль в формировании персистенции данных патогенов в носоглотке при хроническом аденоидите играет способность бактерий к образованию биопленок. Бактериальные биопленки, а также факт обнаружения большого количества бактерий внутри ткани глоточной миндалины, обусловливают возникновение дискуссии о возможностях системной и топической антибактериальной терапии.
Ключевые слова: хронический аденоидит, бактериальная микрофлора, Staphylococcus aureus, Haemophilus influenzae, Streptococcus pneumoniae.
Хронический аденоидит (ХА) — полиэтиологическое заболевание с преобладающей симптоматикой постназального синдрома (post-nasal drip). В его основе лежит нарушение иммунных процессов глоточной миндалины. При этом отсутствует единое мнение о длительности воспалительного процесса, при котором указанные изменения можно считать хроническими. С учетом того, что оториноларингологи не рассматривают ХА как отдельную нозологическую форму, а выделяют лишь гипертрофию аденоидных вегетаций или, при наличии воспалительных изменений в носоглотке, хронический риносинусит, наиболее корректно говорить о ХА в случае сохранения клинической симптоматики заболевания более 12 нед [1].
Несмотря на высокую частоту встречаемости, эпидемиологических данных по патологии носоглотки у детей не так много, и все они достаточно противоречивы. Ввиду частого использования термина «хронический аденоидит» конкретные цифры о распространенности этой патологии можно найти только в русскоязычной литературе. Так, по данным отечественных авторов, доля детей с ХА составляет от 3 [2] до 50% [3] в общей детской популяции и до 70% в группе часто болеющих детей [4].
По современным представлениям, несмотря на главенствующую роль вирусов, в этиологии ХА достаточно большое значение придают хронической бактериальной инфекции. Согласно результатам последних исследований, одним из маркеров хронической бактериальной инфекции являются бактериальные биопленки. Биопленка (от англ. biofilm) представляет собой микробное сообщество, состоящее из клеток, которые прикреплены к поверхности или друг к другу и покрыты экзополисахаридным слоем (гликокаликсом), вырабатываемым самими микробами. По данным B. Winther и соавт., на поверхности удаленных аденоидов бактериальные биопленки были обнаружены в 8 из 9 случаев [5]. В работе итальянских оториноларингологов при исследовании 16 образцов небных миндалин и аденоидов и 24 образцов слизистой оболочки, взятой при вскрытии клеток решетчатого лабиринта у пациентов с хроническим риносинуситом, биопленки были обнаружены в 57,5 и 41,7% случаев, соответственно [6]. В отличие от ХА роль бактерий в гипертрофии аденоидных вегетаций дискутабельна. В частности, по данным J. Coticchia и соавт., у пациентов с ХА биопленки были обнаружены в 94,9% случаев, тогда как на образцах ткани глоточной миндалины, удаленной у пациентов с синдромом обструктивного апноэ сна, — только в 1,9% [7]. Способность бактериальных патогенов к образованию биопленок во многом обусловливает неэффективность антибактериальной терапии при попытке плановой санации носоглотки. При этом считают, что клинические признаки обострения хронического процесса связаны с увеличением количества планктонных форм бактерий, подавление роста которых можно считать обоснованием применению антибактериальных средств [8, 9].
Важным вопросом в настоящее время остается вид основного бактериального патогена при ХА у детей. По мнению одних исследователей, им является Streptococcus pneumoniae (пневмококк) [10, 11]. Согласно другим, главенствующие бактериальные патогены при ХА — это представители грамотрицательной флоры Haemophilus influenzae и Moraxella catarrhalis. По данным I. Brook и соавт., при исследовании материала c поверхности глоточной миндалины наиболее часто обнаруживали H. influenzae (64,4%), M. catarrhalis (35,6%) [12]. В другом исследовании у детей с ХА гемофильная палочка обнаружена в 66,7% случаев [13]. Однако наибольшее число авторов указывают на ведущую роль Staphylococcus aureus в развитии ХА у детей. К примеру, по данным C. D. Lin и соавт., S. aureus был наиболее часто выделяемым патогеном (21,2%) из носоглотки у детей с ХА [14]. По данным M. Emaneini и соавт. [15], частота идентификации S. aureus составила 23%. Согласно результатам отечественных исследований, частота обнаружения S. aureus при исследовании материала с поверхности глоточной миндалины составляет 32%, из ткани — 45%, что уступает только частоте выделения пневмококка [10].
По нашим данным, основным бактериальным патогеном при ХА является золотистый стафилококк, выделяемый с поверхности глоточной миндалины почти у 50% детей. В группе детей с гастроэзофагеальной рефлюксной болезнью частота высевания S. aureus с поверхности глоточной миндалины находится на уровне 70–75% [16]. Регулярный заброс кислого химуса в носоглотку при гастроэзофагеальной рефлюксной болезни приводит к нарушению работы механизмов местного иммунитета (в первую очередь мукоцилиарной системы), что создает благоприятные условия для колонизации и роста патогенной бактериальной микрофлоры (рис.).
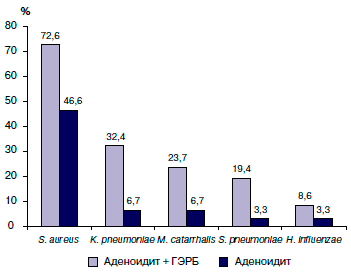
Рис. Частота высеваемости высокопатогенной микрофлоры с поверхности глоточной миндалины у детей с хроническим аденоидитом, ассоциированным и не ассоциированным с гастроэзофагеальной рефлюксной болезнью
Примечание. ГЭРБ — гастроэзофагеальная рефлюксная болезнь.
Согласно последним сведениям, роль грибковой микрофлоры в развитии хронической патологии носоглотки не подтверждена [17]. В отечественной литературе встречаются единичные работы, результаты которых свидетельствуют о вкладе микотической инфекции в развитие ХА. Так, по данным А. И. Мачулина, в 33,3% случаев у детей с ХА имеет место грибково-бактериальная ассоциация [18].
Убедительные фактические данные о значимой роли атипичных возбудителей (Chlamydophila pneumoniae, Mycoplasma pneumoniae) в развитии ХА в настоящее время отсутствуют [17]. Мнения зарубежных исследователей по этому вопросу достаточно противоречивы. Например, в работе G. P. Pintucci и соавт. при исследовании 55 образцов ткани глоточной и небных миндалин M. pneumoniae обнаружены в 10,9% случаев, C. pneumoniae — в 18,2% [19], а в исследовании L. Drago и соавт. в 44 образцах ткани аденоидов C. pneumoniae обнаружены только в 4,8% случаев, тогда как M. pneumoniae не обнаружены вовсе [20].
Вопрос о консервативном лечении ХА достаточно сложен, поскольку не существует каких-либо жестких стандартов его терапии. Лечение ХА, как и любого хронического заболевания, должно быть комплексным, с учетом этиопатогенеза воспалительного процесса [21].
Основным направлением современной фармакотерапии ринологической патологии в настоящее время принято считать противовоспалительную терапию. Наиболее эффективными из существующих средств с противовоспалительным эффектом являются глюкокортикоидные препараты. Так, накоплен клинический опыт применения мометазона фуроата в лечении неаллергической воспалительной ринологической патологии у детей и взрослых [1]. Однако патология носоглотки (гипертрофия аденоидных вегетаций и аденоидит) не входит в официально зарегистрированные показания к применению назального спрея мометазона фуроата.
Вторым по значимости при обсуждении схемы терапии обострений ХА является вопрос об этиотропном лечении. Учитывая главенствующую роль вирусов в развитии ХА, логичным решением было бы активное применение противовирусных средств в лечении и профилактике острых респираторных инфекций. Однако последний анализ рандомизированных клинических исследований показал сомнительную эффективность подавляющего большинства противовирусных препаратов в лечении, и особенно в профилактике острых респираторных инфекций [22].
Учитывая значимую роль патогенной бактериальной микрофлоры при обострении ХА (в особенности при гнойных его формах), необходимо обсудить вопрос о применении антибактериальных средств. При неосложненной форме аденоидита (и даже при гнойной форме, по мнению отечественных авторов) назначение системных антибактериальных лекарственных препаратов не является целесообразным [9, 23, 24]. По нашему мнению, показаниями к проведению системной антибактериальной терапии при ХА можно считать:
- осложненные формы гнойных аденоидитов (острый средний отит, острый бактериальный риносинусит);
- гнойный аденоидит с выраженным снижением качества жизни ребенка (нарушение сна) при неэффективности топической противовоспалительной терапии.
В таких ситуациях хороший эффект дают как препараты кларитромицина и азитромицина, имеющие высокий уровень биодоступности в ткани миндалин, так и защищенных аминопенициллинов [21].
Как уже было сказано выше, при неосложненных формах обострения ХА в педиатрической практике предпочтение отдают антибактериальным препаратам для местного применения. Учитывая значимую роль S. aureus и Klebsiella pneumoniae как ведущих бактериальных патогенов при ХА у детей, большой интерес представляют топические антибактериальные препараты, имеющие в своей основе антибиотики аминогликозидного ряда. Среди трех назальных спреев — растворов антибиотиков, представленных на российском рынке, два содержат в качестве основного действующего вещества именно аминогликозиды. Так, назальный спрей монокомпонентного раствора фрамицетина Изофра обладает высокой активностью против основных бактерий, играющих роль в этиологии ХА. При этом раствор фрамицетина имеет высокий профиль безопасности применения, обусловленный крайне низкой системной биодоступностью, и является единственным в России назальным спреем раствора антибиотика, разрешенным к применению с первых дней жизни ребенка [25]. Не менее эффективен другой назальный спрей аминогликозидного антибиотика, представленный на российском фармрынке, — комплексный препарат раствора неомицина, полимиксина B, дексаметазона и фенилэфрина «Полидекса с фенилэфрином». Для пациентов с хроническим аденоидитом уникальность данного лекарственного средства заключается в комбинации антибактериального компонента (неомицин + полимиксин B) и дексаметазона — глюкокортикоида, обладающего сильнейшим противовоспалительным эффектом. Наличие в составе деконгестанта фенилэфрина позволяет использовать его даже в качестве монотерапии в течение первых дней обострения ХА на фоне острой респираторной инфекции. Важнейшим моментом является и тот факт, что Полидекса с фенилэфрином — единственный в России назальный спрей, содержащий глюкокортикоидный компонент, у которого в официальных показаниях упоминается патология носоглотки. Однако врачам необходимо помнить о высоком уровне системной биодоступности дексаметазона, что ограничивает длительность использования данного препарата (не более 7–10 сут) и обусловливает наличие определенных возрастных ограничений (запрещено применять у детей младше 2,5 лет) [26].
Таким образом, проблема хронических форм патологии носоглотки у детей является одной из наиболее актуальных в современной оториноларингологии и педиатрии, требующей дальнейшего изучения с целью определения единой клинически обоснованной тактики лечения. Вопрос о роли антибактериальных препаратов, как топических, так и системных, также требует дальнейших клинических исследований для разработки единых общепринятых стандартов с формулированием показаний к применению и схемы антибактериальной терапии при обострении хронического аденоидита у детей.
Список литературы
- Fokkens W., Lund V., Mullol J., Bachert C., Alobid I., Baroody F., Cohen N., Cervin A., Douglas R., Gevaert P., Georgalas C., Goossens H., Harvey R., Hellings P., Hopkins C., Jones N., Joos G., Kalogjera L., Kern B., Kowalski M., Price D., Riechelmann H., Schlosser R., Senior B., Thomas M., Toskala E., Voegels R., Wang de Y., Wormald P. J. European position paper on rhinosinusitis and nasal polyps 2012 (EP3OS). Rhinology. 2012; 50 (23): 1–299.
- Цветков Э. А., Веселов Н. Г., Агаджанова С. Н. Социаль ногигиеническая характеристика лорпатологии у детей, посещающих дошкольные учреждения Санкт-Петербурга. Вестн. оториноларингол. 1996; 6: 33–37.
- Рымша М. А., Чаукина В. А. Хронические воспалительные заболевания глотки у детей. Болезни уха, горла и носа в детском возрасте: нац. рук-во. Под ред. М. Р. Богомильского, В. Р. Чистяковой. М.: ГЭОТАР-Медиа. 2008. С. 336–356.
- Маккаев Х. М. Хронический аденотонзиллит у детей как проблема педиатрии и детской оториноларингологии. Росс. вестн. перинатол. и педиатрии (приложение). 2002. С. 7–11.
- Winther B., Gross B.C., Hendley J. O., Early S. V. Location of bacterial biofilm in the mucus overlying the adenoid by light microscopy. Arch. Otolaryngol. Head Neck Surg. 2009; 145 (12): 1239–1245.
- Calo L., Passali G. C., Galli J., Fadda G., Paludetti G. Role of biofilms in chronic inflammatory diseases of the upper airways. Adv. Otorhinolaryngol. 2011; 72: 93–96.
- Coticchia J., Zuliani G., Coleman C. Carron M., Gurrola J., Haupert M., Berk R. Biofilm surface area in the pediatric nasopharynx. Arch. Otolaryngol. Head Neck Surg. 2007; 133 (2): 110–114.
- Marzouk H., Aynehchi B., Thakkar P., Abramowitz T., Goldsmith A. The utility of nasopharyngeal culture in the management of chronic adenoiditis. Int. J. Pediatr. Otorhinolaryngol. 2012; 76 (10): 1413–1415.
- Тулупов Д. А., Карпова Е. П., Воропаева Е. А. Новый взгляд на профилактику и лечение хронического аденоидита у детей. Вестн. оториноларингол. 2011; 1: 66–69.
- Русецкий Ю. Ю., Седых Т. К., Чернышенко И. О., Смирнова В. А. Сравнительное бактериологическое исследование микрофлоры поверхности и биоптатов миндалин у детей с патологией лимфоаденоидного кольца. Педиатрия. 2012; 91 (2): 52–56.
- Niedzielski A., Korona-Glowniak I., Malm A. High prevalence of Streptococcus pneumoniae in adenoids and nasopharynx in preschool children with recurrent upper respiratory tract infections in Poland — distribution of serotypes and drug resistance patterns. Med. Sci. Monit. 2013; 19: 54–60.
- Brook I., Shah K. Bacteriology of adenoids and tonsils in children with recurrent adenotonsillitis. Ann. Otol., Rhinol. Laryngol. 2001; 110 (9): 844–888.
- Nistico L., Kreft R., Gieseke A. Coticchia J. M., Burrows A., Khampang P., Liu Y., Kerschner J. E., Post J. C., Lonergan S., Sampath R., Hu F. Z., Ehrlich G. D., Stoodley P., Hall-Stoodley L. Adenoid reservoir for pathogenic biofilm bacteria. J. Clin. Microbiol. 2011; 47 (4): 1411–1420.
- Lin C. D., Tsai M. H., Lin C. W., Ho M. W., Wang C. Y., Tsou Y. A., Kao M. C., Tsai M. H., Lai C. H. Association of adenoid hyperplasia and bacterial biofilm formation in children with adenoiditis in Taiwan. Eur. Arch. Otorhinolaryngol. 2012; 269 (2): 503–511.
- Emaneini M., Khoramrooz S. S., Taherikalani M., Jabalameli F., Aligholi M. Molecular characterization of Staphylococcus aureus isolated from children with adenoid hypertrophy: Emergence of new spa types t7685 and t7692. Int. J. Pediatr. Otorhinolaryngol. 2011; 75 (11): 1446–1449.
- Тулупов Д. А., Карпова Е. П., Захарова И. Н., Солдатский Ю. Л., Вагина Е. Е. Профилактика хронического аденоидита у детей с кислотозависимой патологией желудка. Вестн. оториноларингол. 2009; 5: 55–58.
- Marseglia G. L., Caimmi D., Pagella F., Matti E., Labo E., Licari A., Salpietro A., Pelizzo G., Castellazzi A. M. Adenoids during childhood: the facts. Int. J. Immunopathol. Pharmacol. 2011; 24 (4): 1–5.
- Мачулин А. И., Кунельская В. Я. Влияние распространенности микобиоты у детей с хроническим аденоидитом. В кн.: Успехи медицинской микологии. Т. 10. Под ред. Ю. В. Сергеева. М.: Национальная академия микологии. 2007. С. 179–181.
- Pintucci J. P., Corno S., Garotta M. Biofilms and infections of the upper respiratory tract. Eur. Rev. Med. Pharmacol. Sci. 2010; 14 (8): 683–690.
- Drago L., Esposito S., Vecchi E., Marchisio P., Blasi F., Baggi E., Capaccio P., Pignataro L. Detection of respiratory viruses and atypical bacteria in children’s tonsils and adenoids. J. Clin. Microbiol. 2008; 46 (1): 369–370.
- Тулупов Д. А., Карпова Е. П. Хронический аденоидит у детей. Пособие для врачей. М.: Петроруш. 2012.
- Jefferson T. O., Tyrrell D. WITHDRAWN: Antivirals for the common cold. Cochr. Database Syst. Rev. 2007; 18 (3): CD002743.
- Шиленкова В. В. Рациональный подход к диагностике и лечению заболеваний носоглотки у детей. Нов. здравоохранения (Ярославль). 2002; 2: 28–32.
- Карпова Е. П. Возможности топической терапии хронического аденоидита у детей. Тез. 11-го Росс. нац. конгр. «Человек и лекарство». 2004. 663 с.
- Allegaert K., Langhendries J. P., van den Anker J. N. Educational paper: do we need neonatal clinical pharmacologists? Eur. J. Pediatr. 2013; 172 (4): 429–435.
- Wolthers O. D. Relevance of pharmacokinetics and bioavailability of intranasal corticosteroids in allergic rhinitis. Recent Pat. Inflamm. Allergy Drug Discov. 2010; 4 (2): 118–123.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
