Кишечная палочка неустойчива к
29.07.2019 00:19
Штаммы уропатогенной кишечной палочки могут длительно сохраняться в кишечниках здоровых женщин и вызывать бактериурию

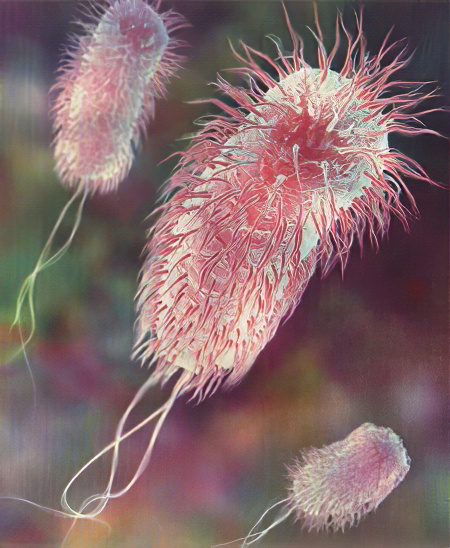
На рисунке: Раскрашенное изображение (полученное с помощью растрового электронного микроскопа) уропатогенных Е. coli, эпителия и нейтрофилов на поверхности слизистой оболочки мочевого пузыря.
Пандемическая уропатогенная устойчивая к фторхинолонам кишечная палочка Escherichia coli обладает повышенной способностью сохраняться в кишечнике и вызывать бактериурию у здоровых женщин
Прим. ред.: Бактериурия – это наличие бактерий в моче. Бактериурия, сопровождаемая симптомами, является инфекцией мочевыводящих путей, в тоже время есть и бессимптомная бактериурия. Диагноз ставится путем анализа мочи или посева мочи. Кишечная палочка Escherichiacoli является наиболее распространенной бактерией при бактериурии.
В конце страницы, в рамках рассматриваемой темы, см. также результаты более раннего исследования об антиадгезионной терапии (альтернаьтиве антибиотикотерапии), которая может уменьшить колонизацию уропатогенной Escherichiacoli.
ИССЛЕДОВАНИЕ
Исследование более 1000 здоровых женщин без симптомов инфекции мочевыводящих путей показало, что почти 9% носили в кишечнике штаммы Escherichia coli с множественной лекарственной устойчивостью. Дополнительные результаты указывают на вероятные причины пандемии резистентных штаммов E.coli. Они показывают ценность проверки статуса пациента-носителя для прогнозирования резистентных инфекций, а также необходимость переосмысления клинического значения бактерий в моче без симптомов, поскольку пандемические штаммы могут быть высокопатогенными для мочевыделительной системы и устойчивыми к лечению.
Это вызывает клиническую озабоченность, поскольку болезнетворные бактерии E. coli могут переноситься из пищеварительного тракта в женский мочевой тракт через мочеиспускательный канал, который короче и расположен по-разному у женщин, чем у мужчин. Затем бактерии могут попасть в мочевой пузырь и другие части мочевыводящих путей.
Более трети образцов мочи, предоставленных теми, кто имел устойчивую к фторхинолонам (Ципро) кишечную кишечную палочку, дали положительный результат на рост E. coli. Из них около 77% были Ципро-устойчивы, и клональный тип бактерий соответствовал образцу кала.
Большая часть обнаруженной патогенной кишечной палочки принадлежала к пандемическим клональным группам ST131-H30R или ST1193 с множественной лекарственной устойчивостью, которые в настоящее время вызывают большинство лекарственно-устойчивых инфекций мочевыводящих путей и кровотока. Они были обнаружены в два раза чаще в моче людей, у которых эти специфические штаммы были в кишечнике, по сравнению с другими штаммами кишечной палочки E. coli в целом.
Кроме того, присутствие группы ST ST131-H30R в кишечнике в этом исследовании было связано с более старшим возрастом.
Исследователи также проверили, какие участники могли иметь назначение антибиотиков во время исследования для любого типа инфекции, включая респираторную.
Через три месяца после этого более раннего сбора мочи инфекции мочевыводящих путей были диагностированы почти в 7% из 45 ранее бессимптомных носителей, которые дали согласие на последующее электронное медицинское обследование. Участники исследования были из района Пьюджет-Саунд (Puget Sound).
«Два пандемических фторхинолон-резистентных патогенных штамма E. coli, обнаруженных в клинических образцах, являются превосходными колонизаторами кишечника и, как правило, сохраняются там», – отметили исследователи. «Они также могут обнаруживаться с необычно высокой частотой в моче здоровых женщин, у которых не было документированного диагноза инфекции мочевыводящих путей во время тестирования образцов. Оба явления, по-видимому, взаимосвязаны».
Исследователи отметили, что уже давно известно, что микробная флора кишечника пациента часто содержит штаммы, вызывающие инфекцию мочевыводящих путей. Не было точно установлено, имеют ли пандемические, лекарственно-устойчивые штаммы отчетливые паттерны (очаги) в кишечнике или нижних мочевых путях здоровых людей.
Исследование было опубликовано в журнале Oxford University Press Journal, Clinical Infectious Diseases («Клинические Инфекционные Заболевания»).
По словам Евгения Сокуренко, профессора микробиологии в Медицинской школе Вашингтонского университета (UW), полученные результаты могут иметь несколько клинических последствий для лечения и инфекционного контроля. Он был старшим научным сотрудником по исследованию. Несколько других преподавателей микробиологии UW и исследователей Постоянного НИИ Кайзера в Сиэтле (Kaiser Permanent Research Institute investigators in Seattle) сотрудничали в этой работе. Ведущим научным сотрудником была Вероника Леонидовна Чеснокова, заведующая кафедрой микробиологии Медицинской школы UW.
Результаты показывают, что определенные штаммы кишечной палочки с множественной лекарственной устойчивостью, обнаруженные в этом исследовании, занимают гораздо более длительное пребывание в кишечнике, чем некоторые другие устойчивые штаммы, а также могут присутствовать в моче здоровых женщин, не вызывая жжения, крови в моче или других предупреждающих признаков бактериальной инфекции.
Сокуренко объяснил, что знание того, присутствуют ли в кишечнике женщины множественные лекарственно-устойчивые штаммы, может помочь предсказать профиль резистентности последующей клинической инфекции. Усилия по избавлению от пандемических штаммов кишечной палочки в кишечнике носителей могут снизить частоту возникновения множественных лекарственно-устойчивых инфекций и, возможно, защитить их домашние или другие контакты.
Сокуренко также сказал, что медицине, возможно, потребуется пересмотреть клиническую значимость обнаружения бактерий в моче, даже без симптомов, во время этой пандемии множественных устойчивых к антибиотикам штаммов E. coli, поскольку эти штаммы могут подвергнуть носителей риску возникновения трудно поддающегося лечению бактериального заболевания.
Фторхинолоны являются наиболее часто назначаемыми препаратами при инфекциях мочевыводящих путей. Несмотря на усилия по ограничению их использования, согласно исследователям, штаммы, устойчивые к этой категории антибиотиков, процветают и распространяются по всему миру.
Исследователи предположили, что превосходная способность двух пандемических штаммов, ST131-H30R и ST119, длительно занимать место в кишечнике людей, возможно, способствовала их быстрому глобальному распространению. Они могут сохраняться и передаваться среди здоровых людей даже в отсутствие применения антибиотиков, что может нарушить микробную структуру кишечной флоры.
Ученые пришли к выводу, что это исследование выдвигает на первый план вероятные физиологические причины пандемии этих устойчивых штаммов кишечной палочки. Оно также указывает на ценность определения статуса носителя у пациенток для прогнозирования будущих резистентных инфекций, а также на необходимость переосмысления клинического значения бактерий, присутствующих в моче без симптомов, особенно с учетом того, что эти пандемические штаммы могут быть супербактериями: высокопатогенными для мочевой системы и устойчивыми к лечению.
Источник: Материалы предоставлены Вашингтонским университетом медицинских наук – University of Washington Health Sciences / UW Medicine
Статья в журнале: Veronika L Tchesnokova, Evgeni V Sokurenko, etal. Pandemic uropathogenic fluoroquinolone-resistant Escherichia coli have enhanced ability to persist in the gut and cause bacteriuria in healthy women. ClinicalInfectiousDiseases, 2019
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
У уропатогенной кишечной палочки понизили способность «прилипать» к эпителию кишечника

На рисунке: Ингибиторы адгезии (красные точки) связываются пилями бактерий, препятствуя их соединению с рецепторами клеток организма-хозяина
Выборочное истощение уропатогенных штаммов E. coli из кишечника с помощью ингибирующего высокоаффинного маннозида
Инфекции мочевыводящих путей (ИМП), вызванные уропатогенной кишечной палочкой (UPEC), поражают 150 миллионов человек ежегодно. Несмотря на эффективную терапию антибиотиками, у 30–50% пациентов наблюдаются рецидивирующие ИМП. Кроме того, растущая распространенность UPEC, которые устойчивы к антибиотикам последней линии, а в последнее время к карбапенемам и колистину, делает ИМП ярким примером кризиса устойчивости к антибиотикам и подчеркивает необходимость новых подходов к лечению и профилактике бактериальных инфекций. Штаммы UPEC устанавливают резервуары в кишечнике, из которых они выделяются с фекалиями, и могут колонизировать периуретральную область или влагалище и впоследствии подниматься через мочеиспускательный канал к мочевыводящим путям, где они вызывают ИМП.
Известно, что бактериальные пили (ворсинки) играют жизненно важную роль в взаимодействиях организма-хозяина и E. coli, опосредуя прикрепление (адгезию) к эпителиальным клеткам мочевого пузыря и почек. Однако в настоящее время недостаточно информации о механизмах колонизации и устойчивости UPEC в кишечнике.
Молекулы адгезии выносятся на поверхность бактерии и собираются с помощью системы секреции chaperon-usher (‘Chaperon-usher pathway’, сокращенно — CUP). Она состоит из двух белков. Один из них получил английское название «chaperone», которое переводится как «компаньон», «сопровождающее лицо», а в транскрипции — «шаперон», а второй компонент получил английское название «usher», которое переводится как «швейцар», «привратник», в транскрипции – «ашер».
Изоляты UPEC кодируют до 16 различных пилей пути CUP, и каждый тип пилей может обеспечивать колонизацию среды обитания в хозяине или окружающей среде.
В исследовании 2017 года, результаты которого опубликованы в журнале Nature, американские ученые продемонстрировали, что механизм шаперон-ашер (CUP) играет роль в колонизации кишечника штаммами UPEC. В частности, авторы создали девять бактерий с одиночными делециями (отсутствующими участками ДНК), у каждого из которых отсутствовал один из генов, кодирующих белки CUP. Эффект этих мутаций тестировали в модели колонизации кишечника мыши. Обнаружилось, что одиночная делеция двух генов, fim и ucl, которые кодируют пили типа 1 и пили типа F17, соответственно, вызвали заметное снижение способности бактерии колонизировать кишечник. Более того, удаление обоих генов в одном штамме приводило к большему дефекту, чем одиночная делеция, что доказывает, что их роли не являются вырожденными.
Операторы fim и ucl кодируют адгезины, которые расположены на дистальном конце каждой ворсинки. Эти адгезины, FimH и UclD, соответственно, опосредуют связывание с клетками организма-хозяина. Путем тестирования очищенных фрагментов этих двух адгезинов в анализах in vitro авторы продемонстрировали четкую специфичность связывания с гликанами, присутствующими на поверхности эпителиальных клеток хозяина, располагающимися в криптах кишечной стенки; FimH связан преимущественно с N-связанными гликанами, которые содержат маннозу (т.е. адгезин пилей типа 1 FimH в дальнейшем связывает маннозу на поверхности мочевого пузыря и опосредует колонизацию мочевого пузыря), тогда как UclD связаны с O-связанными гликанами.
В предыдущих исследованиях было показано, что потеря пилей типа 1 отразилась в потере способности UPEC колонизировать мочевой пузырь. Чтобы попытаться предотвратить связывание пилей типа 1 с эпителиальными клетками кишечника, авторы протестировали маннозид M4284, который представляет собой небольшую синтетическую молекулу, которая связана с маннозой и связывается с адгезином FimH пилей 1 типа с высокой аффинностью.
Прим. ред.: Справедливости ради стоит отметить, что уже ранее (судя по публикациям), для целей терапии рецидивирующих инфекций мочеполовых путей, вызываемых уропатогенными штаммами E.coli, рассматривалось применение маннозидов, т.е. D-маннозы, которая чаще встречается именно в виде «маннозидов» – гликозидов, содержащих маннозу. В свободном же состоянии D-манноза, которая представляет 1 из 2-х стереоизомеров маннозы (т.е. и есть сама манноза) лишь иногда встречается в некоторых растениях (в Amorphophallus Konjac, в кожуре апельсинов), при этом, D-манноза является основным стереоизомером маннозы, встречающимся в природе. Однако в описываемом исследовании речь идет о тестировании более эффективного варианта маннозида, что указывает на возможность более успешной антиадгезионной терапии.
У мышей, которые перорально получали это соединение, произошло снижение колонизации кишечника штаммами UPEC по сравнению с контрольной группой. То есть этот маннозид может эффективно конкурировать за связывание с маннозой на клетках хозяина и, таким образом, непосредственно вмешиваться во взаимодействие “хозяин-патоген”. Авторы также показывают, что введение маннозида может снизить вероятность развития ИМП путем одновременного удаления UPEC из кишечника и лечения активной инфекции мочевого пузыря.
Исследование показало, ингибирующий высокоаффинный маннозид, уменьшает кишечную колонизацию генетически разнообразных изолятов UPEC, одновременно обрабатывая ИМП, без заметного нарушения структурной конфигурации микробиоты кишечника. Избирательно истощая резервуары UPEC в кишечнике, маннозиды могут заметно снизить частоту ИМП и рецидивирующих ИМП.
Иными словами, лечение не вызывало существенных изменений в составе микробиоты кишечника, в отличие от применяемых в настоящее время антибиотиков. Таким образом, антиадгезионная терапия может уменьшить колонизацию конкретными бактериями и представляет собой альтернативу антибиотикотерапии.
Источник: Caitlin N. Spaulding. et al. Selective depletion of uropathogenic E. coli from the gut by a FimH antagonist. Nature 546, 529–532 (2017)
Об адгезии микроорганизмов (в т.ч. про “пили”, “фимбрии”, адгезины и т.д.) см. дополнительно в подразделе Адгезия микроорганизмов: общие сведения
Пожалуйста, авторизуйтесь, чтобы оставить комментарий.
Источник
Причины и симптомы кишечной палочки
Что такое кишечная палочка?
Кишечная палочка (Escherichia coli, E. coli) является палочковидной бактерией, принадлежащей к группе факультативных анаэробов (живет и размножается только в условиях отсутствия прямого кислорода). Кишечная палочка имеет множество штаммов, большинство из которых принадлежит к естественной микрофлоре кишечника людей и помогает предотвращать развитие вредоносных микроорганизмов и синтезировать витамин К. Однако некоторые её разновидности (например, серотип О157:Н7) способны вызвать серьезные отравления, кишечный дисбактериоз и колибактериоз.
Нормальная микрофлора кишечника включает в себя множество микроорганизмов, среди которых – лактобактерии, энтерококки, стрептококки и проч. Штаммы этих бактерий находятся в равновесии, но если последнее каким-либо образом нарушится, патогенные микроорганизмы начнут усиленно размножаться. При этом активизируются процессы брожения и гниения, вызывая развитие серьезных заболеваний.
Некоторые штаммы кишечной палочки вызывают не только заболевания желудочно-кишечного тракта, но поражают также мочеполовую систему, провоцируют кольпит, цистит, простатит, менингит у младенцев, иногда становятся причиной развития гемолитически-уремического синдрома, перитонита, мастита, пневмонии и сепсиса.
Причины заболеваний, вызванных кишечной палочкой
Нарушения пищеварения, размножение патогенного серотипа кишечной палочки и дисбактериоз могут возникать из-за многих заболеваний пищеварительной системы, в особенности поджелудочной железы (панкреатиты) и кишечника (колиты, энтероколиты).
Помимо этого, нарушить нормальную микрофлору кишечника может приём некоторых антибиотиков, подавляющих те микроорганизмы, которые отвечают за предотвращение размножения патогенной флоры.
Чтобы избежать дисбактериоза и расстройств пищеварения, необходимо правильно подбирать антибактериальные препараты, их дозу и те медикаменты, которые будут защищать нормальную микрофлору кишечника.
Заражение патогенными штаммами кишечной палочки происходит преимущественно фекально-оральным путем. Способствует развитию заболеваний нарушение правил гигиены приготовления пищи, употребление грязных фруктов и овощей, использование воды для полива, загрязненной или сточной. Опасно также есть плохо прожаренное мясо или пить некипяченое молоко, ведь коровы, козы, свиньи и овцы могут быть носителями патогенных штаммов E. coli.
Симптомы кишечной палочки
Пищевые отравления, вызванные некоторыми штаммами кишечной палочки, опасны из-за выделяемых ими токсинов. Некоторые из этих токсинов являются потенциально смертельными. Обнаруживают патогенные микроорганизмы в слизистых желудочно-кишечного тракта и воспаленных тканях (очагах воспаления).
Симптомами кишечной палочки становится развернутая клиническая картина кишечного дисбактериоза: помимо расстройств стула (запоры, поносы), у больного наблюдаются тошнота и рвота, вздутие и боль в животе. Меняется запах каловых масс, появляется неприятный запах изо рта. Среди симптомов общей интоксикации – повышенная утомляемость, слабость, сонливость, отсутствие аппетита.
Избавление от кишечной палочки
Лечение кишечной палочки заключается в приеме специально подобранных антибиотиков. Чаще всего это препараты из группы аминогликозидов. Чтобы лечение было более эффективным, больному рекомендуется сделать посев содержимого кишечника. Если кишечная палочка вызвала диарею, необходимо восстановление водно-электролитного баланса с помощью регидратации. В целом, лечение зависит в первую очередь от штамма кишечной палочки.

Автор статьи: Мочалов Павел Александрович | д. м. н. терапевт
Образование:
Московский медицинский институт им. И. М. Сеченова, специальность – “Лечебное дело” в 1991 году, в 1993 году “Профессиональные болезни”, в 1996 году “Терапия”.
Наши авторы
Источник
4106 просмотров
1 декабря 2016
После отравления за границей не могу вылечить дисбактериоз, вызванный гемолитической E.coli 10 в 7-ой степени. Сдавала анализ кала на дисбактериоз 4 раза в двух разных лабораториях. После первого раза лечить ничем не стала, т.к. сдала потом анализ повторно и ничего не нашли. После второго и третьего раза помимо кишечной палочки в анализе находили другие бактерии (E.coli лактозонегативная 10 в 3, золотистый стафилокок). E.coli была чувствительна к цефтриаксону,цефотаксиму,цефалотину,хлорамфениколу,доксициклину,цефуроксиму,ампициллину. Лечилась бактисубтилом, альфанормиксом, бифиформом.
Последняя проверка показала,что кишечная палочка устойчива ко всем антибиотикам (амоксициллину,клавулановой кислоте,доксициклину, ко-тримоксазолу,налидиксовойкислоте,цефиксиму,цефотаксиму,ципрофлоксацину) и бактериофагам,используемым в лаборатории.Также,нашли протеи sp. 10 в 6-ой степени ( они ко всем вышесказанным антибиотикам чувствительны (кроме, ко-тримоксазолу)) и сниженное число лактобактерий ,также 10 в 6-ой степени.
Подскажите пожалуйста чем вылечить дисбактериоз? Хочу попробовать эрсефурил (как советовала когда-то инфекционист). Будет ли от него толк и нужно ли что-то принимать совместно с антибиотиком?
Заранее большое спасибо!
На сервисе СпросиВрача доступна консультация гастроэнтеролога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Педиатр, Терапевт, Массажист
Бактериофаг интести, завязывайте с антибитиками, они больше калечат. Новые пробиотики Флувир или Према.

Педиатр, Терапевт, Массажист
Елена, 2 декабря 2016
Клиент
Наталья, спасибо большое за ответ! К сожалению, к интестифагу, колипротейному фагу и поливалентному пиобактериофагу она тоже устойчива (исходя из анализов)

Педиатр, Терапевт, Массажист
А вы пропейте он комбинированный, результат может быть хорошим. Еще эрсефурил- тот же фурозолидон, он энтеросептик. Его пропить 10 дней стоит. Фурозолидон дешевле по моему- по 2 т – 4р. 10 дней. Очень хороший.

Педиатр, Терапевт, Массажист
А ваш дисбактериоз клинически как проявляется? Если потравить патологическую флору не получается, попробуйте ее выселить- флувир или према, и хилакфорте для лучшего приживления. Пропить фуразолидон, или ко- тримоксазол 10 дней. Затем интести 10 дней, вместе с флувир или премой с хилакфорте месяц. Вот такой стратегический план.
Елена, 2 декабря 2016
Клиент
Честно говоря, он никак не проявляется. Только на основе анализов. Я просто решила периодически делать анализ на дисбактериоз,т.к. один раз у меня эта же гемолитическая палочка попала в мочу, я её вылечила и боюсь,что она снова может попасть туда

Педиатр, Терапевт, Массажист
Легче пропить уроваксом, для профилактики урологических инфекций,чем лечить кишечник.
Оцените, насколько были полезны ответы врачей
Проголосовал 1 человек,
средняя оценка 5
Что делать, если я не нашел ответ на свой вопрос?
Если у Вас похожий или аналогичный вопрос, но Вы не нашли на него ответ – получите свою 03 онлайн консультацию от врача эксперта.
Если Вы хотите получить более подробную консультацию врача и решить проблему быстро и индивидуально – задайте платный вопрос в приватном личном сообщении. Будьте здоровы!
Источник
