Обмен белков желудочно кишечном тракте
Переваривание белков в желудочно-кишечном тракте
Переваривание белков начинается в желудке под действием ферментов желудочного сока. За сутки его выделяется до 2,5 литров и он отличается от других пищеварительных соков сильно кислой реакцией, благодаря присутствию свободной соляной кислоты, секретируемой обкладочными клетками слизистой желудка.
Секреция соляной кислоты представляет активный транспорт, осуществляемый протонной АТФ-азой с затратой АТФ.
Роль соляной кислоты:
1. денатурирует белки;
2. стерилизует пищу;
3. вызывает набухание труднорастворимых белков;
4. активирует пепсиноген;
5. создает рН-оптимум для действия пепсина;
6. способствует всасыванию железа;
7. вызывает секрецию секретина в двенадцатиперстной кишке.
В желудочном соке содержатся протеолитические ферменты пепсин, гастриксин и реннин. Главным из них является пепсин. Он вырабатывается главными клетками слизистой желудка в виде профермента пепсиногена. Активация его осуществляется соляной кислотой (медленная) и аутокаталитически пепсином (быстрая) путем отщепления фрагмента полипептидной цепи с N-конца (частичный протеолиз). При этом происходит изменение конформации молекулы и формирование активного центра. Пепсин действует при значениях рН 1,5–2,5 и является эндопептидазой с относительной специфичностью действия, расщепляющей пептидные связи внутри белковой молекулы.
Кроме пепсина в желудочном соке содержится фермент гастриксин, проявляющий протеолитическую активность при рН 3,0–4,0. По-видимому, именно он начинает переваривание белков.
В желудочном соке грудных детей содержится фермент реннин, который имеет большое значение для переваривания белков у грудных детей, т.к. катализирует створаживание молока (превращение растворимого казеиногена в нерастворимый казеин), в результате чего замедляется продвижение нерастворимого казеина в двенадцатиперстную кишку и он дольше подвергается действию протеаз.
Образовавшиеся в результате действия пепсина в желудке полипептиды поступают в двенадцатиперстную кишку, куда выделяется сок поджелудочной железы. Панкреатический сок имеет щелочную реакцию (рН 7,5–8,2), что обусловлено высоким содержанием бикарбонатов. Кислое содержимое, поступающее из желудка нейтрализуется, и пепсин теряет свою активность.
В панкреатическом соке содержатся протеолитические ферменты трипсин, химотрипсин, карбоксипептидаза и эластаза, которые вырабатываются также в виде проферментов. Трипсиноген активируется энтерокиназой (вырабатывается клетками слизистой двенадцатиперстной кишки), переходит в активный трипсин, который активирует все остальные ферменты поджелудочного и кишечного сока. Клетки поджелудочной железы защищены от действия протеаз тем, что ферменты желудочного сока образуются в виде неактивных предшественников, а в панкреас синтезируется особый белок-ингибитор трипсина. В полости ЖКТ протеазы не контактируют с белками клеток, поскольку слизистая оболочка покрыта слоем слизи, а каждая клетка содержит на наружной поверхности плазматической мембраны полисахариды, которые не расщепляются протеазами. Разрушение клеточных белков ферментами желудочного или кишечного сока происходит при язвенной болезни.
Переваривание продуктов протеолиза пищевых белков в тонком кишечнике осуществляется с помощью амино-, ди-, и трипептидаз, которые функционируют преимущественно пристеночно.
Таким образом, конечными продуктами переваривания белков в ЖКТ являются свободные аминокислоты, которые всасываются.
Данный текст является ознакомительным фрагментом.
Похожие главы из других книг:
Изменения белков[43]
Те участки генома, которые кодируют белки, изменились на удивление мало. Различия в аминокислотных последовательностях белков у человека и шимпанзе составляют значительно менее 1 %, да и из этих немногочисленных различий большая часть либо не имеет
Глава 2. Строение и функции белков
Белки – высокомолекулярные азотсодержащие органические соединения, состоящие из аминокислот, соединенных в полипептидные цепи с помощью пептидных связей, и имеющие сложную структурную организацию.История изучения белковВ 1728 г.
Уровни структурной организации белков
Первичная структура – строго определенная линейная последовательность аминокислот в полипептидной цепочке.Стратегические принципы изучения первичной структуры белка претерпевали значительные изменения по мере развития и
Функционирование белков
Каждый индивидуальный белок, имеющий уникальную первичную структуру и конформацию, обладает и уникальной функцией, отличающей его от всех остальных белков. Набор индивидуальных белков выполняет в клетке множество разнообразных и сложных
Посттрансляционные изменения белков
Многие белки синтезируются в неактивном виде (предшественники) и после схождения с рибосом подвергаются постсинтетическим структурным модификациям. Эти конформационные и структурные изменения полипептидных цепей получили
Переваривание углеводов
В слюне содержится фермент ?-амилаза, расщепляющая ?-1,4-гликозидные связи внутри молекул полисахаридов.Переваривание основной массы углеводов происходит в двенадцатиперстной кишке под действием ферментов панкреатического сока – ?-амилазы,
Глава 19. Липиды тканей, переваривание и транспорт липидов
Липиды – неоднородная в химическом отношении группа веществ биологического происхождения, общим свойством которых является гидрофобность и способность растворяться в неполярных органических растворителях.
Липиды пищи, их переваривание и всасывание.
Взрослому человеку требуется от 70 до 145 г липидов в сутки в зависимости от трудовой деятельности, пола, возраста и климатических условий. При рациональном питании жиры должны обеспечивать не более 30% от общей калорийности
Расщепление белков в тканях
Осуществляется с помощью протеолитических лизосомальных ферментов катепсинов. По строению активного центра выделяют цистеиновые, сериновые, карбоксильные и металлопротеиновые катепсины. Роль катепсинов:1. создание биологически активных
Распад нуклеиновых кислот в желудочно-кишечном тракте и тканях
Нуклеиновые кислоты поступают в организм с пищей главным образом в составе нуклеопротеинов и высвобождаются в результате действия протеолитических ферментов желудочно-кишечного тракта. Далее под
Характеристика белков сыворотки крови
Белки системы комплемента – к этой системе относятся 20 белков, циркулирующих в крови в форме неактивных предшественников. Их активация происходит под действием специфических веществ, обладающих протеолитической активностью.
Глава 4. Нарушения нормальных функций желудочно-кишечного тракта
Различные нарушения в работе желудочно-кишечного тракта могут быть как временными, так и длительными, возникшими в результате болезни. В обоих случаях владельцу собаки трудно самому установить причину
5
Болезни желудочно-кишечного тракта
Собаки – животные плотоядные. Тем не менее, их организм приспособился к потреблению и усвоению питательных веществ рациона, состоящего из смеси различных кормов.
В процессе пищеварения белки, жиры и углеводы пищи подвергаются
Желудочно-кишечный тракт
Строение пищевода и однокамерного желудка собаки – стандартное для хищников. 12-перстная кишка висит на короткой брыжейке. От пилорической части желудка она отходит в правое подреберье, направляется вдоль печени по правой стенке брюшной полости
3.8. Защитные системы желудочно-кишечного тракта
Теория адекватного питания придает большое значение системам защиты организма от проникновения различных вредных веществ в его внутреннюю среду. Поступление пищевых веществ в желудочно-кишечный тракт следует
3.8. Защитные системы желудочно-кишечного тракта
Теория адекватного питания придает большое значение системам защиты организма от проникновения различных вредных веществ в его внутреннюю среду. Поступление пищевых веществ в желудочно-кишечный тракт следует
Источник
Расщепление белков до аминокислот начинается в желудке, продолжается в двенадцатиперстной кишке и заканчивается в тонком кишечнике. В некоторых случаях распад белков и превращения аминокислот могут происходить также в толстом кишечнике под влиянием микрофлоры.
Протеолитические ферменты подразделяют по особенности их действия на экзопептидазы, отщепляющие концевые аминокислоты, и эндопептидазы, действующие на внутренние пептидные связи.
В желудке пища подвергается воздействию желудочного сока, включающего соляную кислоту и ферменты. К ферментам желудка относятся две группы протеаз с разным оптимумом рН, которые упрощенно называют пепсин и гастриксин. У грудных детей основным ферментом является реннин.
Регуляция желудочного пищеварения
Регуляция осуществляется нервными (условные и безусловные рефлексы) и гуморальными механизмами. К гуморальным регуляторам желудочной секреции относятся гастрин и гистамин.
Гастрин секретируется специфичными G-клетками пилорического отдела:
- в ответ на раздражение механорецепторов,
- в ответ на раздражение хеморецепторов (продукты первичного гидролиза белков),
- под влиянием n.vagus.
Далее гастрин через системный кровоток достигает и стимулирует главные, обкладочные и добавочные клетки, что вызывает секрецию желудочного сока, в большей мере соляной кислоты. Также он обеспечивает секрецию гистамина, влияя на ECL-клетки (enterochromaffin-like cells, англ. энтерохромаффиноподобные клетки).
Гистамин, образующийся в энтерохромаффиноподобных клетках слизистой оболочки желудка (фундальные железы), выходит в кровоток, взаимодействует с Н2-рецепторами на обкладочных клетках и увеличивает в них синтез и секрецию соляной кислоты.
Закисление желудочного содержимого (pH 1,0) по механизму обратной отрицательной связи подавляет активность G-клеток, снижает секрецию гастрина и желудочного сока.
Соляная кислота
Одним из важнейших компонентов желудочного сока является соляная кислота. В образовании соляной кислоты принимают участие париетальные (обкладочные) клетки желудка, секретирующие ионы Н+. Источником ионов Н+ является угольная кислота, образуемая ферментом карбоангидразой. При ее диссоциациии , кроме ионов водорода, образуются карбонат-ионы НСО3–. Они по градиенту концентрации движутся в кровь в обмен на ионы Сl–. В полость желудка ионы Н+ попадают энергозависимым антипортом с ионами К+ (Н+,К+-АТФаза), хлорид-ионы перекачиваются в просвет желудка также с затратой энергии.
Н+,К+-АТФаза (протонная помпа) является мишенью действия лекарственных препаратов “ингибиторов протонной помпы” – омепразол, пантопразол и др., используемых для лечения заболеваний желудочно-кишечного тракта, связанных с повышенной кислотностью (гастриты, язвы желудка и 12-перстной кишки, дуоденит).
При нарушении нормальной секреции HCl возникают гипоацидный или гиперацидный гастрит, отличающиеся друг от друга по клиническим проявлениям, последствиям и требуемой схеме лечения.
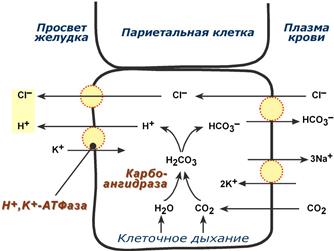
Синтез соляной кислоты
Функции соляной кислоты
- Денатурация белков пищи.
- Бактерицидное действие.
- Высвобождение железа из комплекса с белками, что необходимо для его всасывания. Аналогично высвобождаются и другие металлы.
- Высвобождение различных органических молекул, прочно связанных с белковой частью (гем, коферменты – тиаминдифосфат, ФАД, ФМН, пиридоксальфосфат, кобаламин, биотин), что позволяет витаминам впоследствии всасываться.
- Превращение неактивного пепсиногена в активный пепсин.
- Снижение рН желудочного содержимого до 1,5-2,5 и создание оптимума рН для работы пепсина.
- После перехода в 12-перстную кишку – стимуляция секреции кишечных гормонов и, следовательно, выделения панкреатического сока и желчи.
Кислая реакция желудочного сока обусловлена, главным образом, присутствием HCl, гораздо в меньшей степени иона H2PO4-, при патологиях (гипо- и анацидное состояние, онкология) свой вклад может вносить молочная кислота.
Совокупность всех веществ желудочного сока, способных быть донорами протонов, составляет общую кислотность. Соляную кислоту, находящуюся в комплексе с белками, мукополисахаридами слизистой оболочки и продуктами переваривания, называют связанной соляной кислотой, оставшуюся часть – свободной соляной кислотой. Содержание свободной HCl подвержено изменениям, в то же время количество связанной HCl относительно постоянно.
Влияние гастрина и гистамина на обкладочные клетки сводится к усилению работы Н+,К+-АТФазы. Действие гастрина заключается в активации кальций-фосфолипидного механизма передачи сигнала, гистамин действует по аденилатциклазному механизму.
Изменение кислотности в желудке
Гипоацидное состояние развивается при снижении активности и/или количества обкладочных клеток, синтезирующих HCl. В результате могут развиваться самые разнообразные последствия, прямо или косвенно связанные с невыполнением соляной кислотой ее функций:
- снижение переваривания белков как в желудке, так и в кишечнике,
- активация процессов брожения в желудке, запах изо рта,
- активация процесса гниения белков в толстой кишке, бурление в кишечнике и метеоризм,
- проникновение недопереваренных продуктов в кровь и, как следствие, аллергические реакции,
- уменьшение высвобождения от белков и возникновение дефицита минеральных веществ (железо, медь, магний, цинк, йод и др),
- снижение высвобождения от белков и всасывания ряда водорастворимых витаминов – развитие гиповитаминозов (B1, B2, B6, B12, H),
- снижение синтеза обкладочными клетками внутреннего фактора Касла и снижение всасывания витамина B12,
- снижение секреции кишечных гормонов и, как следствие, уменьшение выделения желчи и панкреатического сока,
- нарушение переваривания и всасывания липидов и, как следствие, развитие гиповитаминозов по жирорастворимым витаминам.
Гиперацидное состояние развивается при повышенной активности обкладочных клеток. Может приводить к клиническим проявлениям в виде воспаления стенки желудка, эрозии и язвенной болезни желудка и двенадцатипеперстной кишки.
Пепсин
Пепсин является эндопептидазой, то есть он расщепляет внутренние пептидные связи в молекулах белков и пептидов. Синтезируется в главных клетках желудка в виде неактивного профермента пепсиногена, в котором активный центр “прикрыт” N-концевым фрагментом. При наличии соляной кислоты конформация пепсиногена изменяется таким образом, что “раскрывается” активный центр фермента, который отщепляет остаточный пептид (N-концевой фрагмент), т.е. происходит аутокатализ. В результате образуется активный пепсин, активирующий и другие молекулы пепсиногена.
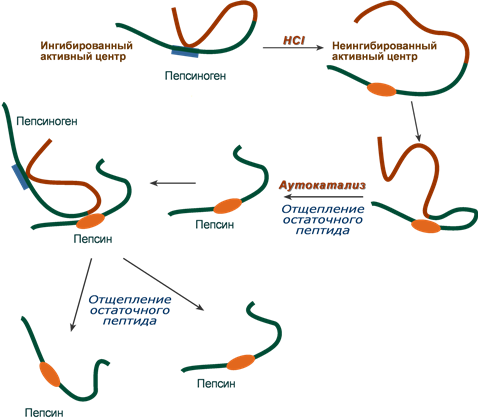
Превращение пепсиногена в пепсин
Пепсин обладает невысокой специфичностью, в основном он гидролизует пептидные связи, образованные аминогруппами ароматических аминокислот (тирозина, фенилаланина, триптофана), меньше и медленнее – аминогруппами и карбоксигруппами лейцина, глутаминовой кислоты и т.д. Оптимум рН для работы пепсина 1,5-2,0.
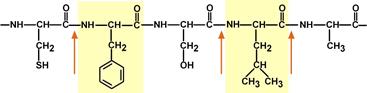
Связи, расщепляемые пепсином
Гастриксин
Гастриксин по своим функциям близок к пепсину, его количество в желудочном соке составляет 20-50% от количества пепсина. Синтезируется главными клетками желудка в виде прогастриксина (профермент) и активируется соляной кислотой. Оптимум рН гастриксина соответствует 3,2-3,5 и значение этот фермент имеет при питании молочно-растительной пищей, слабее стимулирующей выделение соляной кислоты и одновременно нейтрализующей ее в просвете желудка. Гастриксин является эндопептидазой и гидролизует связи, образованные карбоксильными группами дикарбоновых аминокислот.
В течение суток синтезируется около 2 г пепсина. Объем работы пепсина составляет примерно 10% от всех пептидных связей белков, попадающих в желудок.
Наличие в желудке двух протеаз, действующих при различных pH, позволяет организму пепсином переваривать белки мясной пищи, стимулирующей секрецию HCL, а гастриксином – белки растительно-молочной пищи.
Источник
Обмен белков – совокупность пластических и энергетических процессов превращения белков в организме, включая обмен аминокислот и продуктов их распада. Белки – основа всех клеточ-ных структур, являются материальными носителями жизни. Биосинтез белков определяет рост, развитие и самообновление всех структурных элементов в организме и тем самым их функциональную надежность. Суточная потребность в белках (белковый оптимум) для взрослого человека составляет 100-120 г (при трате энергии 3000 ккал/сутки). В распоряжении организма должны быть все аминокислоты (20) в определенном соотношении и количестве, иначе белок не может быть синтезирован. Многие составляющие белок аминокислоты (валин, лейцин, изолейцин, лизин,метионин, треонин, фенилаланин, триптофан) не могут синтезироваться в организме и должны поступать с пищей (незаменимые аминокислоты). Другие аминокислоты могут быть синтезированы в организме и называются заменимыми (гистидин,гликокол,глицин,аланин, глутаминовая кислота, пролин, оксипролин, серии, тирозин, цистеин, аргинин,).Белки делят на биологически полноценные (с полным набором всех незаменимых аминокислот) и неполноценные (при отсутствии одной или нескольких незаменимых аминокислот).
Основные этапы обмена белков:1) ферментативное расщепление белков пищи до аминокислот и всасывание последних;2) превращение аминокислот;3) биосинтез белков;4) расщепление белков; 5) образование конечных продуктов распада аминокислот.
Всосавшись в кровеносные капилляры ворсинок слизистой оболочки тонкого кишечника, аминокислоты по воротной вене поступают в течень,где они немедленно используются, либо задерживаются в качестве небольшого резерва. Часть аминокислот остается в крови и попадает в другие клетки тела, где они включаются в состав новых белков. Белки тела непрерывно расщепляются и синтезируются заново (период обновления общего белка в организме – 80 дней). Если пища содержит больше аминокислот, чем необходимо для синтеза клеточных белков, ферменты печени отщепляют от них аминогруппы NH2, т.е. производят дезаминирование. Другие ферменты, соединяя отщепленные аминогруппы с СО2, образуют из них мочевину, которая переносится с кровью в почки и выделяется с мочой. Белки не откладываются в депо, поэтому белки, которые организм расходует после истощения запаса углеводов и жиров, – не резервные, а ферменты и структурные белки клеток.
Нарушения обмена белков в организме могут быть количественные и качественные. О количественных изменениях белкового обмена судят по азотистому балансу, т.е. по соотношению количества азота, поступившегo в организм с пищей и выделенного из него. В норме у взрослого человека при адекватном питании количество введенного в организм азота равно количеству, выведенного из организма (азотистое равновесие). Когда поступление азота превышает его выде-ление, говорят о положительном азотистом балансе, при этом происходит задержка азота в орга-низме. Наблюдается в период роста организма, во время беременности, при выздоровлении.. Когда количество выведенного из организма азота превышает количество поступившего, говорят об отрицательном азотистом балансе.Он отмечается при значительном снижении содержания белка в пище (белковом голодании).
Азотистый баланс – разница между количеством азота, поступающего с пищей, и количеством азота, выделяемого почками в виде мочевины и азотистых солей. Он является показателем состояния белкового и аминокислотного обмена.
Азотистый баланс может быть:
• положительным – у детей, беременных женщин, при увеличении мышечной массы у спортсменов и больных, выздоравливающих после тяжелой болезни, что свидетельствует о преобладании синтеза белков и роста тканей над их распадом;
• отрицательным – при тяжелых заболеваниях, голодании, старении, что свидетельствует об усилении процессов распада белков;
• равным нулю (азотистое равновесие) – у здоровых взрослых людей при нормальном питании.
При переваривании происходит гидролиз пищевых белков до свободных аминокислот. Процесс переваривания начинается в желудке и продолжается в тонком кишечнике под действием ферментов пептидгидролаз (пептидаз). Основные пептидазы синтезируются в клетках желудка, поджелудочной железы и кишечника. В желудке белки пищи денатурируются и гидролизуются с образованием олигопептидов. Вкишечнике панкреатические пептидазы продолжают гидролиз олигопептидов до ди- и трипептидов и свободных аминокислот. Короткие пептиды расщепляются до свободных аминокислот в пристеночном слое или в клетках кишечного эпителия. Затем происходит их всасывание.
Все пептидазы, в зависимости от места расположения в пептиде гидролизуемой связи, делятся на эндопептидазы и экзопептидазы:
• эндопептидазы – расщепляют пептидные связи, удаленные от концов пептидной цепи (пепсин, трипсин, химотрипсин, эластаза);
• экзопептидазы – гидролизуют пептидные связи, образованные N- и С-концевыми аминокислотами (аминопептидаза, карбоксипептидазы А и В), а также расщепляют ди- и трипептиды.
Рис. 9.1. Переваривание белков в желудочно-кишечном тракте
Ферменты, участвующие в переваривании белков, обладают относительной субстратной специфичностью и гидролизуют пептидные связи; при этом каждая пептидаза преимущественно расщепляет связи, образованные определенными аминокислотами (табл. 9.1).
2.Желудочные и панкреатические пептидазы вырабатываются в неактивной форме (проферменты), секретируются к месту действия, где активируются путем частичного протеолиза (отщепление пептида различной длины, чаще с N-конца молекулы профермента). Место синтеза проферментов (клетки слизистой оболочки желудка, поджелудочная железа) и место их активации (полость желудка, тонкого кишечника)пространственно разделены. Такой механизм образования активных ферментов необходим для защиты секреторных клеток желудка и поджелудочной железы от самопереваривания.
Таблица 9.1. Характеристика протеолитических ферментов желудочно-кишечного тракта
Примечание: X – любая аминокислота
Преждевременная активация проферментов в секреторных клетках происходит при:
• язвенной болезни желудка – пепсиноген превращается в пепсин в клетках слизистой желудка;
• остром панкреатите – трипсиноген превращается в трипсин в клетках поджелудочной железы и активирует остальные панкреатические пептидазы.
Всасывание продуктов гидролиза белков. Белки после гидролиза до аминокислот всасываются в кишечнике. Всасывание различных аминокислот в разных отделах тонкой кишки происходит с различной скоростью. Всасывание аминокислот из полости кишки в ее эпителиоциты осуществляется активно с участием переносчика и с затратой энергии АТФ. Из эпителиоцитов аминокислоты по механизму облегченной диффузии транспортируются в межклеточную жидкость. Всосавшиеся в кровь аминокислоты попадают по системе воротной вены в печень, где подвергаются различным превращениям. Значительная часть аминокислот используется для синтеза белка. Аминокислоты в печени дезаминируются, а часть подвергается ферментному переаминированию. Разнесенные кровотоком по всему организму аминокислоты служат исходным материалом для построения различных тканевых белков, гормонов, ферментов, гемоглобина и других веществ белковой природы. Некоторая часть аминокислот используется как источник энергии.
Интенсивность всасывания аминокислот зависит от возраста – более интенсивно оно в молодом возрасте, от уровня белкового обмена в организме, от содержания в крови свободных аминокислот, от нервных и гуморальных влияний.
Источник
