Рост кишечной палочки на среде левина
Эшерихии (кишечная палочка)
История открытия.
Впервые были выделены из кишечника ребенка и описаны в 1885 г. немецким врачом-педиатром Теодором Эшерихом.
Таксономия. Семейство | Enterobacteriaceae |
Триба | Escherichieae |
Род | Escherichia |
Виды | E. сoli и другие, всего 5 видов |
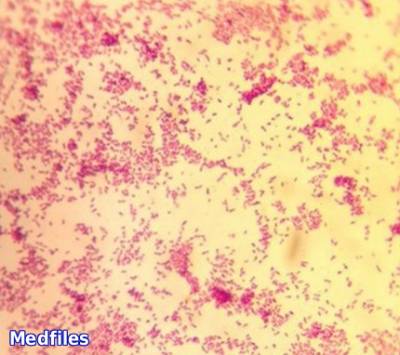
Морфология и тинкториальные свойства.
E. сoli представляют собой грамотрицательные прямые с закругленными концами палочки размером 0,4-0,-2-6 мкм, в мазках располагаются беспорядочно, подвижные (перетрихи), имеют микрокапсулу, пили I и II типов, спор не образуют.
Культуральные свойства.
E.сoli – факультативные анаэробы, хемоорганогетеротрофы. Не требовательны к условиям культивирования. Оптимальные условия культивирования: температура 37 С, рН 7,2-7,5, длительность культивирования – 24-48 часа. Хорошо растут на простых питательных средах (МПБ, МПА). В МПБ наблюдается рост в виде диффузного помутнения с последующим образованием осадка. На МПА образуют колонии в S-форме: слабовыпуклые полупрозрачные колонии с ровными краями и гладкой, блестящей поверхностью среднего размера. Возможен рост в R-форме (колонии с изрезанными краями, шероховатой поверхностью), иногда вырастают слизистые колонии (М-форма).
Дают характерный рост на дифференциально-диагностических средах: Эндо (малиновые колонии с металлическим блеском); Левина (темно-синие колонии с металлическим блеском), Плоскирева (розовые колонии с металлическим блеском), Ресселя и Олькеницкого. На кровяном агаре могут давать гемолиз.
Биохимические свойства.
E. сoli обладают высокой ферментативной активностью. Каталазоположительны и оксидазоотрицательны. Реакция Фогеса-Проскауэра отрицательная. Разлагают сахара (глюкозу, лактозу, маннит, арабинозу, сахарозу и др.) до кислоты и газа. Разложение лактозы до кислоты и газа является отличительным признаком эшерихий от других энтеробактерий. Восстанавливают нитраты в нитриты, образуют индол, аммиак, не продуцируют сероводород, не разжижают желатин.
Антигенная структура.
Антигенная структура сложная. Имеются О-, Н-, К- (L, В, А), М-антигены, фимбриальные, рибосомные и многие другие антигены. При сероидентификации наибольшее значение имеют О-, Н-, К- антигены.
* О – соматический антиген, липополисахарид клеточной стенки, термостабильный, спиртоустойчивый, групповой (?171 серогруппа).
* Н – жгутиковый антиген, белок флагеллин , типовой (более 57 серотипов).
* К – капсульный антиген , кислый полисахарид, тоже типовой (более 97 серотипов). К-антиген не однороден – в зависимости от устойчивости к температуре выделяют 3 его разновидности :
– L – термолабильный антиген (разрушается при нагревании до 600С);
– А – термостабильный (выдерживает 2-3-часовое кипячение);
– В – промежуточный по термолабильности между А и L (выдерживает нагревание до 60С в течение часа, но разрушается при кипячении).
Серовары эшерихий обозначают с указанием антигенной формулы: О26:К60: Н2…
Факторы патогенности.
1. Токсины:
* эндотоксин – оказывает на организм человека пирогенное и токсическое (снижение АД, нейротоксичность) действие, подавляет фагоцитоз;
* экзотоксины образуют некоторые штаммы кишечной палочки:
– энтеротоскин (ЭТКП);
– цитотоксин с гемолитическим и некротическим действием (ЭИКП, ЭГКП).
2. Структурные и химические компоненты клетки:
* пили I (адгезия) и II (конъюгация) типов;
* капсула и Т-белок клеточной стенки (адгезия, подавление фагоцитоза);
* плазмиды (у E. сoli обнаружены Col-, R-, F-, Hly-, Ent-плазмиды, а также плазмиды, кодирующие синтез факторов адгезии).
Резистентность.
E. сoli обладают хорошей выживаемостью во внешней среде, сохраняются в почве и воде несколько месяцев. При 56С гибнут в течении 1 часа, нагревание до 60С выдерживают не более 15-20 мин, при кипячении погибают мгновенно. Чувствительны к дезинфицирующим средствам и антибиотикам.
Экология и роль в патологии.
Различают условно-патогенные и диареегенные E. сoli.
Условно-патогенные E. сoli входят в состав микрофлоры кишечника человека, млекопитающих, птиц, рептилий и рыб. С испражнениями E. сoli выделяются в окружающую среду. Кишечная палочка является санитарно-показательным микроорганизмом, ее обнаружение свидетельствует о свежем фекальном загрязнении объектов внешней среды.
Условно-патогенные E. сoli вызывают эндогенные гнойно-воспалительные процессы различной локализации (инфекции мочевыводящих путей, нагноение ран, холецистит, аппендицит, перитонит, конъюктивит, отит, пневмонии, менингиты…) вплоть до сепсиса, чаще на фоне ИДС.
Диареегенные E. сoli являются возбудителями экзогенных инфекций – эшерихиозов (острые кишечные заболевания, протекающие по типу энтеритов и энтероколитов) и пищевые отравления.
Эпидемиология.
Заболевания, вызванные E. сoli, распространено повсеместно.
Источник инфекции: больные и бактерионосители.
Механизм передачи: фекально-оральный (пути: пищевой, контактно-бытовой и реже водный).
Патогенез и клинические проявления.
Диареегенные серовары кишечной палочки разделены на 5 групп:
* Энтеропатогенные (ЭПКП);
* Энтеротоксигенные (ЭТКП);
* Энтероинвазивные (ЭИКП);
* Энтерогеморрагические (ЭГКП);
* Энтероадгезивные (ЭАКП).
Кроме вышеперечисленных выделяют диффузноприлипаемые кишечные палочки (пока недостаточно изучены).
Морфологически представители разных групп не отличимы друг от друга; их дифференцируют по антигенной структуре и по факторам патогенности.
ЭПКП – вызывают эшерихиозы у детей до 1 года (чаще у детей, находящихся на искусственном вскармливании). Возбудители поражают эпителий тонкого кишечника: адсорбируясь на поверхности энтероцитов за счет белка наружной мембраны (интимина), размножаются здесь и повреждают микроворсинки, вызывая их отторжение. Развивающаяся при этом воспалительная реакция обусловлена действием эндотоскина, который освобождается при разрушении кишечных палочек. Основные клинические проявления: диарея, рвота, срыгивание пищи, признаки обезвоживания организма, гипотрофия. Течение болезни – тяжелое, может длиться неделями.
ЭТКП вызывают холероподобные заболевания у детей и взрослых. При помощи пилей они прикрепляются к эпителию нижних отделов тонкого кишечника, размножаются благодаря CF (фактор колонизации) и продуцируют 2 типа токсинов: LT (термолабильный, по механизму действия напоминает экзотоксин холерного вибриона) и ST (термостабильный). LT и ST увеличивают в клетках эпителия содержание цАМФ и цГМФ соответственно, что вызывает нарушение транспорта молекулярного железа и повышенному выходу воды из клеток. Это нарушает водно-солевой баланс в кишечнике и приводит к развитию водянистой диареи. Заболевание по характеру течения напоминает легкую форму холеры (в литературе его часто называют диареей путешественников).
ЭИКП вызывают дизентериеподобное заболевание у детей и взрослых. Адсорбируются на клетках эпителия нижних отделов толстой кишки, проникают внутрь клеток, размножаются, выделяют шигеллоподобный токсин и разрушают клетки. Распространяясь по межклеточным пространствам, они поражают соседние клетки, образуя язвы. Клинические симптомы: вначале – водянистая диарея, затем в испражнениях появляется примесь слизи и крови.
ЭГКП – возбудители геморрагической диареи и гемолитического уремического синдрома, поражая преимущественно детей. Возбудители выделяют шигелоподобный цитотоксин, вызывающий разрушение эндотелия сосудов (блокирует синтез белков на рибосомах) кишечника и почек, в результате чего развиваются ишемия и некроз клеток. Клинически наблюдается геморрагический колит (кровавый понос) и гемолитический уремический синдром (гемолитическая анемия и почечная недостаточность), которые протекают тяжело и нередко с летальным исходом.
ЭАКП (описаны в 1985 г.у) способны быстро прикрепляться к поверхности клеток и колонизировать разные отделы кишечника, но чаще поражают толстую кишку. Цитотоксинов они не образуют, в клетки не проникают. Клинически заболевание характеризуется упорным диарейным синдромом.
Иммунитет.
После перенесения эшерихиозов формируется гуморальный типоспецифический иммунитет, наблюдается выработка местного иммунитета (SIgA). Образующие антитела не обладают протективными свойствами.
У детей первого года жизни пассивный трансплацентарный иммунитет обеспечивается проходящими через плаценту антителам и антителам, поступающими с материнским молоком. Также с женским молоком передаются и мукополисахариды, способствующие размножению лакто- и бифидобактерий – антагонистов возбудителей эшерихиозов.
Микробиологическая диагностика.
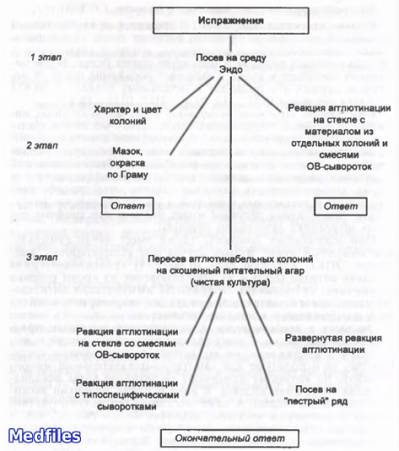
Исследуемый материал: при кишечных эшерихиозах – испражнения, рвотные массы, у грудных детей мазки из зева, при эндогенной инфекции – материал из соответствующего очага (моча, отделяемое раны, кровь…).
1. Бактериоскопический метод.
2. Бактериологичекий метод (основной) – выделение чистой культуры возбудителя, ее идентификация, определение чувствительности к антибиотикам.
3. Серологический метод:
* РА с поли-(ОВ) и моновалентными агглютинирующими эшерихиозными сыворотками;
* ИФА;
* РИФ.
4. Молекулярно-биологический метод (ПЦР, ДНК-зонды).
Специфическая профилактика не разработана.
Неспецифическая профилактика: ранняя диагностика, изоляция больных, регулярное профилактическое обследование работников детских учреждений и ЛПУ. Большое значение имеет строгое соблюдение санэпидрежима в этих учреждениях.
Принципы терапии: диета, ХТП (нитрофураны, фторхинолоны), при генерализованных формах – антибиотики с учетом чувствительности, спецефическое лечение – коли-бактериофаг, лакто- и бифидосодержащие пробиотики.
Источник
ЛЕВИНА СРЕДА (M. Levine, амер. бактериолог, род. в 1889 г.; син. агар с эозином и метиленовым синим) — цветная элективная питательная среда для дифференцирования бактерий сем. Enterobacteriaсеае, используется при лабораторной диагностике дизентерии, брюшного тифа, сальмонеллезов и других кишечных инфекций. Впервые агар с эозином и метиленовым синим был предложен в 1916 г. Холт-Харрисом и Тигом (J. E. Holt-Harris, О. Teague), позднее, в 1918 г., состав среды был модифицирован Левином.
Л. с. наряду с другими твердыми цветными дифференциально-диагностическими питательными средами для энтеробактерий нашла широкое применение в лаб. практике. С ее помощью удается в сравнительно большом проценте случаев обнаружить патогенную лактозонегативную микрофлору. Готовая Л. с. довольно стабильна, не изменяет своих свойств на свету или при хранении на протяжении нескольких дней; при ее изготовлении не требуется точного установления концентрации водородных ионов (pH). Входящие в состав Л. с. органические красители избирательно задерживают рост грамположительных бактерий, благодаря чему она одновременно является средой обогащения и дает относительно лучшие результаты при непосредственном посеве исследуемого материала, даже если он содержит сравнительно малое количество патогенных бактерий.
В зависимости от качества отдельных ингредиентов (пептона и в особенности красителей) получаемые на Л. с. результаты могут несколько варьировать, поэтому при изготовлении каждой новой серии среды желательно использование материалов одной и той же марки, что значительно облегчает распознавание колоний.
Известно несколько прописей и способов приготовления Л. с. (Ю. А. Козлов, Г. Я. Синай, О. Г. Биргер и др.). Наибольшее распространение получил способ, при к-ром раздельно готовят основную среду, р-ры лактозы и красителей, пригодные для сохранения впрок и смешиваемые перед употреблением.
Основная среда состоит из 10 г бактериологического пептона, 15 г агар-агара, 2 г фосфата калия двузамещенного (K2HPO4) и 1 л дистиллированной воды. Ее стерилизуют в автоклаве при 1 ат 15—20 мин., pH не исправляют.
При приготовлении дифференциальной среды на каждые 100 мл расплавленной основной среды при постоянном помешивании добавляют приготовленные на дистиллированной воде и предварительно простерилизованные текучим паром (дробно, 3 дня подряд по 15—20 мин.) следующие р-ры в приведенной последовательности 5 мл 20% р-ра медицинской лактозы, 2 мл 2% р-ра эозина щелочного (бактериологического), 1,5 мл 0,5% р-ра метиленового синего. Готовую среду разливают в чашки Петри, слегка подсушивают и используют как обычно. Цвет среды сине-фиолетовый.
Колонии кишечной палочки на Л. с. небольшие, округлые, с гладкой блестящей поверхностью, темно-синего (до черного) цвета, иногда с металлическим блеском. Молодые колонии мутноватые, непрозрачные, могут быть окрашены только в центре. Колонии возбудителей дизентерии, брюшного тифа и паратифов относительно более мелкие, круглые, блестящие и прозрачные, обычно совершенно бесцветные (молодые) или с легким розоватым или голубоватым оттенком. Колонии протея ползучего роста не дают; они небольшие, изолированные, оранжево-желтого цвета. Среда меняет свой цвет только вокруг колоний протея.
Некоторые авторы рекомендуют увеличивать количество 0,5% р-ра метиленового синего до 2 мл на 100 мл основной среды или исключать из ее состава фосфатный буфер. Можно готовить среду не с пептоном, а на основе перевара Хоттингера, при pH 7,2—7,3 с добавлением соответствующего прописи количества агара и фосфорнокислого калия. Применение мясной воды для приготовления среды недопустимо, дифференциация колоний в этом случае значительно ухудшается.
Известен способ приготовления сухой Л. с., очень стабильной по качеству и особенно удобной для длительного хранения и в условиях экспедиционной работы (Н. В. Плоскирев).
Стабильная сухая Л. с. выпускается промышленностью, инструкция по ее изготовлению и применению рассылается вместе со средой. Большинство диагностических лабораторий применяет для выделения и дифференцирования патогенных энтеробактерий высококачественные стандартные элективные сухие питательные среды отечественного производства — Л. с., бактоагар Ж, среду Плоскирева (см. Плоскирева среда).
См. также Дифференциально-диагностические среды, Питательные среды.
Библиография: Руководство по микробиологической диагностике инфекционных болезней, под ред. К. И. Матвеева, с. 110, М., 1973; Справочник по микробиологическим и вирусологическим методам исследования, под ред. М. О. Биргера, с. 58, М., 1973; Levine М. The effect of concentration of dyes on differentiation of enteric bacteria on eosin- methylene- blue agar, J. Bact., v. 45, p. 471, 1943.
Г. П. Беликов.
Источник: Большая Медицинская Энциклопедия (БМЭ), под редакцией Петровского Б.В., 3-е издание
Рекомендуемые статьи
Источник
Для определения сахаролитических свойств микробов применяют дифференциально-диагностические среды такие, как среды Гисса, среда Эндо, среда Левина, среда Плоскирева.
Среды Эндо, Левина, Плоскирева в чашках Петри применяются для дифференцировки бактерий кишечной группы по способности сбраживать лактозу. Эти среды содержат питательный агар, лактозу и индикатор, изменяющий свой цвет в кислой среде (индикатор рН). Если посеять на такую среду бактерии, которые сбраживают лактозу, например, кишечную палочку, то в результате сбраживания лактозы образуется кислота, и индикатор изменит свой цвет в кислой среде. Поэтому колонии кишечной палочки на таких средах будут окрашены соответственно цвету индикатора: на среде Эндо и среде Плоскирева — в красный цвет, на среде Левина — в черно-синий. Если же на эти среды посеять бактерии, которые не сбраживают лактозу, например, палочки брюшного тифа или палочки дизентерии, то кислота не образуется, реакция среды останется слабощелочной и цвет индикатора не изменится. Поэтому колонии бактерий, не сбраживающих лактозу, на этих средах будут бесцветными
Среду Плоскирева можно отнести также и к элективным средам для выделения палочек дизентерии, так как эта среда содержит соли желчных кислот, задерживающих рост кишечной палочки, и краситель бриллиантовый зеленый, задерживающий рост воздушной кокковой микрофлоры.
Висмут-сульфит агар (ВСА) — это дифференциально-диагностическая среда, применяемая главным образом при диагностике сальмонеллезов. При росте сальмонелл происходит восстановление висмута из его солей и колонии сальмонелл окрашиваются в черный цвет.
Дифференциально-диагностические среды Гисса («пестрого» ряда) готовятся на основе жидкой среды (пептонной воды) или полужидкого мясопептонного агара. Содержат какой либо углевод или многоатомный спирт (лактозу, глюкозу, маннит, сахарозу) и индикатор, который меняет свой цвет в кислой среде. В пробирку с жидкой средой Гисса помещен стеклянный поплавок. Если на среду Гисса посеять микроб, который сбраживает данный углевод с образованием кислоты и газа, то есть до конечных продуктов, то среда изменит свой цвет, в полужидкой среде появятся пузырьки и разрывы в толще агара, в жидкой среде — пузырек газа в поплавке. При сбраживании углевода только до промежуточных продуктов (до кислоты) происходит только изменение цвета среды.
4. Методы изучения протеолитических и редуцирующих свойств бактерий.
Для определения протеолитической активности микробы засевают уколом в столбик желатина и после 3-5 суток инкубирования при комнатной температуре отмечают характер разжижения желатина: в виде воронки, гвоздя, чулка или в виде опрокинутой елки. Протеолитическую активность определяют также по образованию продуктов разложения белка: индола, сероводорода, аммиака. Для их определения засевают микроорганизмы в мясопептонный бульон, и между горлышком пробирки и ватной пробкой помещают индикаторные бумажки, исключая их контакт со средой. При образовании индола бумага, пропитанная насыщенным раствором щавелевой кислоты, приобретает розовый цвет; в присутствии сероводорода бумага, пропитанная ацетатом свинца, чернеет; при образовании аммиака красная лакмусовая бумажка синеет.
Для выявления редуцирующих свойств бактерий к обычным питательным средам (мясопептонному бульону, мясопептонному агару, молоку) добавляют соответствующие индикаторы (метиленовую синь, лакмус и др.).
Приводим несколько методов определения редуцирующих свойств.
1.) 5 мл молока с метиленовой синью засевают петлей исследуемой культуры, снятой с плотной питательной среды, или 1,0 мл 18-часовой бульонной культуры. После 24-часовой инкубации в термостате при 27° С отмечают результаты. При положительной реакции среда из голубой становится кремового цвета, а при слабой редукции приобретает зеленоватую окраску.
Молоко с метиленовой синью готовится следующим образом: свежее молоко доводят до кипения, оставляют в прохладном месте на сутки, освобождают его от сливок, затем вторично кипятят и через сутки вновь снимают верхний слой. Обезжиренное таким образом молоко фильтруют через толстый слой ваты, подщелачивают 10%-ным раствором углекислого натрия до pH 7,2. К 100 мл молока добавляют 2 мл 1%-ного водного раствора метиленовой сини. Приготовленную среду разливают по 5 мл в стерильные пробирки и стерилизуют текучим паром три дня подряд по 30 мин. После остывания среда имеет темно-голубой цвет. При наличии у бактерий редуцирующей способности метиленовая синь обесцвечивается и среда приобретает кремовый цвет.
2.) Определение редуцирующей способности бактерий на среде Омелянского производится следующим образом: к 100 мл щелочного мясопептонного агара добавляют десять капель стерильного свежеприготовленного 1%-ного водного раствора метиленовой сини. При посеве бактерий, обладающих редуцирующей способностью, среда обесцвечивается.
3.) На среде Ротбергера выявление редуцирующей способности бактерий состоит в следующем: к 100 мл расплавленного мясопептонного агара добавляют 0,3 г глюкозы и 1 мл насыщенного водорастворимого нейтраль-рота. Разливают в пробирки и дробно стерилизуют, затем среду охлаждают в вертикальном положении. Посев производят уколом. При наличии редуцирующей способности у бактерий цвет среды изменяется – из красного становится желтым (это становится хорошо заметным, если среду покрыть слоем жидкого парафина). При образовании газа в результате расщепления глюкозы агар растрескивается.
5. Использование ферментов (и ферментативной деятельности) микроорганизмов в медицине и биологии.
Для микробов характерна высокая ферментативная активность. Это используется в промышленности для получения органических кислот (уксусной, молочной, щавелевой, лимонной), приготовления молочных продуктов (сыр, ацидофилин, кумыс), в виноделии, пивоварении и других отраслях промышленности. Ферменты микробного происхождения – липазы и протеазы, входящие в состав моющих средств и стиральных порошков, расщепляют белковые и жировые загрязнения до водорастворимых веществ, которые легко смываются водой. В медицине находят применение такие лечебные средства, как стрептокиназа (фибринолизин стрептококков), террилитин (протеаза Aspergillus terricola). Так, во многих клиниках проводят измерение активности различных форм ферментов лактатдегидрогеназы и трансаминазы – их соотношение изменяется при таких болезнях как инфаркт миокарда, поражения печени, мышечные дистрофии; фермент стрептокиназу врачи применяют для рассасывания тромбов; ферменты трипсин и коллагеназа используются для рассасывания рубцов. С помощью ферментов получают витамины, гормоны, алкалозы, веществ, происходящих внутри клетки.
Рекомендуемые страницы:
Воспользуйтесь поиском по сайту:
Источник
