Генная инженерия кишечная палочка
Скромная бактерия за полстолетия с момента ее открытия в конце XIX в. стала настоящей волшебной палочкой для молекулярной биологии. Сейчас результаты опытов с ее использованием занимают главы и тома профессиональных и популярных изданий. Конечно, в нашем путеводителе по модельным организмам E. coli должна была занять свое почетное место.

Двенадцать модельных организмов
Привет! Меня зовут Сергей Мошковский. Дорогая редакция «Биомолекулы», выпустив настенный календарь о модельных организмах на 2020 год, заказала было мне лонгрид, который должен был, как суровый конвой, сопровождать календарь на сайте. Минутная слабость — сколько их было в жизни! — и я уже соглашаюсь. Но как писать? Ведь о каждой модельной скотинке, нарисованной на календаре, — как и о нескольких десятках не поместившихся туда, — написаны тома научной и даже популярной литературы. Придется писать не по-журналистски, из головы — как бы не вышло чего-то вроде поэмы «Москва — Петушки», где вместо станций — модельные организмы. Я и еще несколько авторов представляем вам на суд собранье пестрых глав — они будут выходить в течение всего 2020 года. Читатель, прости! Ты знаешь, кого за это винить!
Escherichia и Eschrichtius — Болезнь путешественников — Главная модельная бактерия — Учебник молекулярной генетики — Невезение с CRISPR/Cas
Кишечная палочка — один из первых мемов, с которым сталкиваются дети при знакомстве с биологией (рис. 1а). Запоминающееся, простое и забавное название. Помню, как узнал в детстве, что эта палочка может быть опасной — кто-то мучился животом, а родители сказали, что, наверное, кишечная палочка! Позже, уже в старшей школе, я узнал латинское название этой бактерии, и оно меня удивило, оказавшись каким-то не очень латинским. Оказывается, австрийский педиатр Теодор Эшерих (рис. 1б), который впервые выделил эту палочку из содержимого кишечника в 1885 году, вначале назвал ее благозвучно — Bacterium coli, что означает просто «кишечная бактерия». После ожидаемого пересмотра классификации бактерий род переименовали в честь первооткрывателя. По анекдотическому совпадению очень созвучно — Eschrichtius — называется одно из самых крупных существ на земле — серый кит (рис. 1в). Правда, этого гиганта так назвали в честь другого ученого — датского зоолога Даниэля Эшрихта, работавшего на полвека раньше (рис. 1г). В этом плане другой важной палочке — сенной — повезло больше, поскольку она до сих пор называется Bacillus subtilis, что в переводе — тонкая палочка.
Рисунок 1а. Escherichia длиной 2 мкм

Рисунок 1б. Теодор Эшерих (1857–1911)

Рисунок 1в. Eschrichtius длиной 14 метров

Рисунок 1г. Даниэль Фредрик Эшрихт (1798–1863)
Кишечная палочка живет… правильно, в кишечнике человека, составляя по численности не более 0,1% нормальной микрофлоры. Как и многие микроорганизмы, эта грамотрицательная палочка очень изменчива и из дружественного — комменсального — компонента микрофлоры кишечника зачастую превращается во вредный — патогенный. Практически каждый сталкивался с «колийной» инфекцией. Например, именно эшерихия вызывает большинство случаев диареи путешественников. В приморских районах местные жители иммунны к штаммам кишечной палочки, населяющим источники воды, поэтому от них страдают туристы. Одним из параметров качества питьевой воды считается косвенный показатель содержания в ней клеток кишечной палочки — так называемый коли-титр. Как и многие патогенные бактерии, кишечная палочка охотно приобретает свойства множественной устойчивости к антибиотикам . Так, в мире растет число случаев возвратного цистита [1] — воспаления мочевого пузыря — и других инфекций, вызванных мультирезистентными штаммами E. coli.
Зачем же такую опасную бактерию сделали модельной? Дело в том, что в условиях культивирования кишечная палочка часто теряет патогенность, становится неспособной жить в естественных для себя условиях (то есть одомашнивается). И этим свойством в 1940-е годы воспользовались микробиологи, проведя с лабораторными штаммами E. coli (например, со знаменитым штаммом К12) много прорывных для науки экспериментов.
Так, манипулируя мутированными штаммами кишечной палочки, которые уже научились получать при помощи облучения, Джошуа Ледерберг и Эдуард Лаури Тейтем в 1947 году обнаружили способность разных штаммов обмениваться генетическим материалом и спасать друг друга от образовавшихся дефектов, проявлявшихся в неспособности расти на минимальной питательной среде. Так был открыт процесс конъюгации бактерий, который затем послужил важным инструментом для картирования бактериального генома . Ведь тогда это можно было делать только косвенными, микробиологическими методами — сама природа генетического кода была неизвестна.
С начала 1950-х годов исследования по молекулярной генетике с использованием кишечной палочки и ее вирусов в качестве основного инструмента росли как снежный ком. Не будет преувеличением сказать, что к 70-м годам E. coli написала учебник молекулярной генетики! Вспомним открытие генетического кода, в котором участвовало несколько коллективов физиков и молекулярных биологов, в том числе Френсис Крик, Георгий Гамов и другие выдающиеся люди того времени [6]. Основные эксперименты по расшифровке кода велись на бесклеточных лизатах кишечной палочки.
Одновременно (или вскоре после этого) с помощью штаммов эшерихии были заложены основы современной молекулярной биологии. Французы Франсуа Жакоб и Жак Моно на примере лактозного оперона — серии генов E. coli, кодирующих каскад расщепления сахара лактозы, — раскрыли механизмы регуляции генной экспрессии — «самовыражения» генетического материала в виде работы белков, в данном случае — ферментов. На материале кишечной палочки описаны все процессы передачи информации в клетке: так называемые матричные процессы — репликация ДНК, транскрипция и трансляция. Я помню, как в университете на микробиологии нам раздали учебники Стента и Кэлиндара по молекулярной генетике, издания, кажется, 1981 года. Вначале было непонятно, почему это нужно для микробиологии, а потом оказалось, что материал учебника — кстати, очень непростой для восприятия второкурсника — на две трети описывает эксперименты, проведенные на кишечной палочке и ее вирусах.
Позднее обнаружилось, что E. coli хорошо подходит для зародившейся в 1960–1970-е годы биотехнологии [7]. Бактерия хорошо переносит введение в свою клетку гетерологичных (то есть чужеродных) генов и во многих случаях способна синтезировать их продукты без вреда для себя. Белки, полученные таким способом, стали называть рекомбинантными, и теперь они широко используются в медицине и других практических задачах.
Кишечная палочка — возможно, самый исследованный организм с точки зрения молекулярной биологии. Тем не менее у элементов ее генома до сих пор обнаруживают новые свойства. Это одновременно плохо (как же мало мы знаем!) и хорошо (будет чем заняться!). Совсем недавно на защите диссертации я услышал о том, как у одной из генных кассет эшерихии, участвующей в каскаде переработки сульфолипидов, также обнаружена и лактазная активность [8]. До этого такая активность была известна только у знаменитого лактозного оперона Жакоба и Моно, описанного в 1961 году!
Кажется, что E. coli — модельный организм без недостатков. Тем не менее биотехнологам не повезло, что у этой бактерии от природы нет системы бактериального иммунитета CRISPR/Cas [9], о которой я уже упоминал в эссе о бактериофаге лямбда [3]. Именно поэтому эту систему, ныне незаменимую в генной инженерии, открыли относительно поздно.
Кишечная палочка-выручалочка — это здорово (рис. 2). Но теперь пора переместиться в мир ядерных организмов. Удобным инструментом для молекулярной биологии и генетики эукариот оказались одноклеточные грибы — дрожжи — и гаплоидный плесневый гриб — нейроспора. Как они дошли до такой одноклеточной и гаплоидной жизни и что было открыто с их помощью — читайте в следующем материале нашего путеводителя по модельным организмам через месяц.
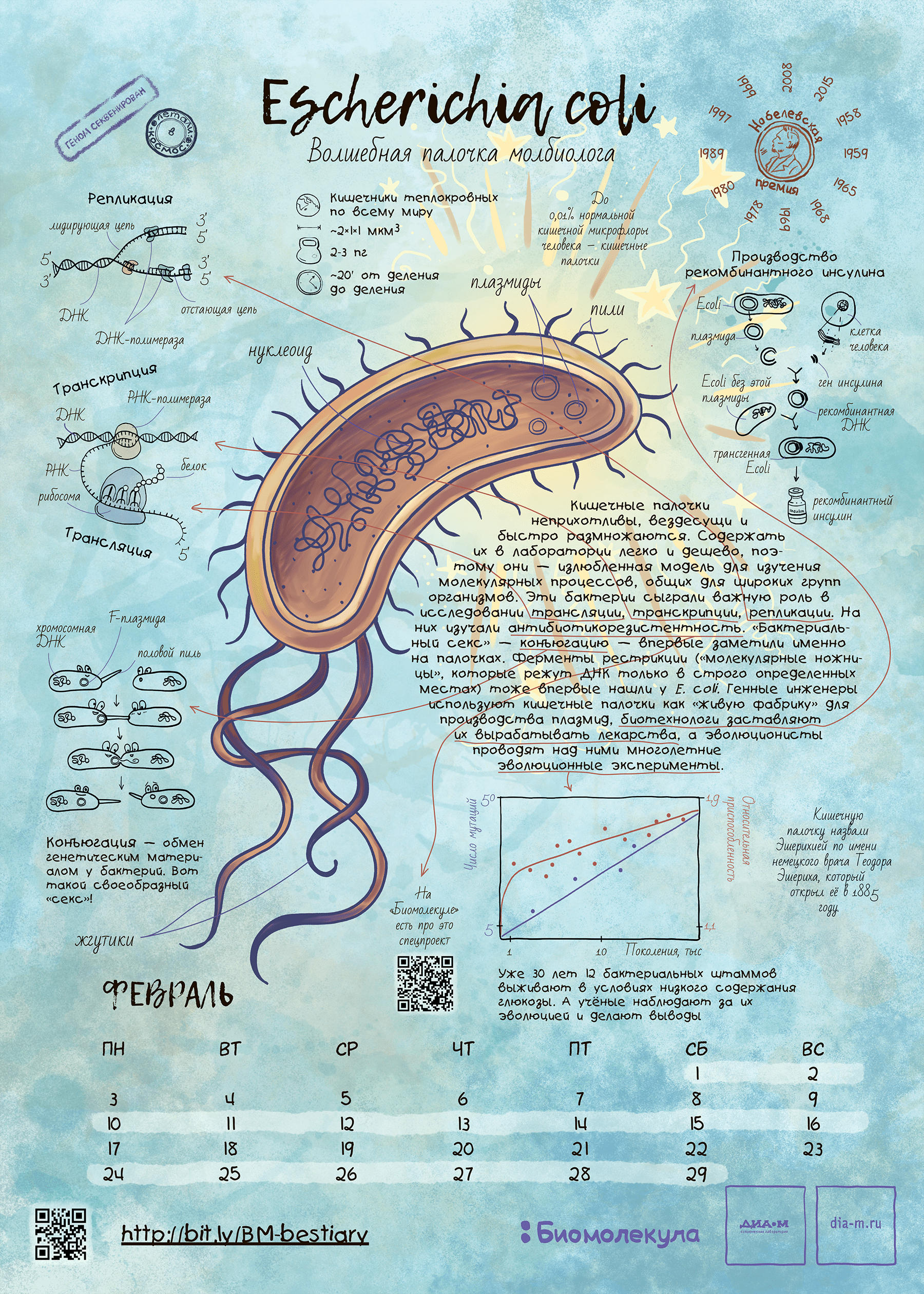
Рисунок 2. Кишечная палочка Escherichia coli как герой календаря «Биомолекулы». Этот календарь мы сделали в 2019 году и даже провели на него весьма успешный краудфандинг. На тех, кто успел приобрести календарь, палочка уже взирает со стенки, ну а с прочими мы делимся хайрезом этого листа — скачивайте, печатайте и вешайте на стенку! Ну а кто все же хочет приобрести бумажный экземпляр — приглашаем в интернет-магазин «Планеты.ру»!
Благодарность
Автор благодарит своего друга — биоинформатика Анну Казнадзей (ИППИ РАН) за ее увлекательный рассказ о новом «лактозном опероне» кишечной палочки, в открытии которого она участвовала.
- Florian Hitzenbichler, Michaela Simon, Thomas Holzmann, Michael Iberer, Markus Zimmermann, et. al.. (2018). Antibiotic resistance in E. coli isolates from patients with urinary tract infections presenting to the emergency department. Infection. 46, 325-331;
- Антибиотики и антибиотикорезистентность: от древности до наших дней;
- Модельные организмы: фаг лямбда;
- 12 методов в картинках: генная инженерия. Часть I, историческая;
- Молекулярная биология;
- У истоков генетического кода: родственные души;
- Биотехнология. Генная инженерия;
- Anna Kaznadzey, Pavel Shelyakin, Evgeniya Belousova, Aleksandra Eremina, Uliana Shvyreva, et. al.. (2018). The genes of the sulphoquinovose catabolism in Escherichia coli are also associated with a previously unknown pathway of lactose degradation. Sci Rep. 8;
- CRISPR-системы: иммунизация прокариот.
Источник
Ðåäàêòèðîâàíèå ãåíîìîâ ðàñòåíèé ìîæåò áóêâàëüíî âñå: íàïðèìåð, «ðàçáóäèòü» â ïîìèäîðàõ ãåí, îòâå÷àþùèé çà îñòðûé âêóñ â ãåíîìå ïåðöà ÷èëè, èëè ïðèäàòü ñàäîâîé êëóáíèêå âêóñ ïåðñèêà Àãðîèíäóñòðèÿ èñïîëüçóåò ãåííî-èíæåíåðíûå òåõíîëîãèè, ÷òîáû ñîçäàòü íå òîëüêî âêóñíûå, íî è áîëåå ïîëåçíûå è óðîæàéíûå êóëüòóðû. Ýòî íåîáõîäèìî, ÷òîáû ïðîêîðìèòü ñòðåìèòåëüíî ðàñòóùåå íàñåëåíèå ïëàíåòû.  Ðîññèè äåéñòâóåò çàêîí, ðàçðåøàþùèé âûðàùèâàòü è ðàçâîäèòü ÃÌÎ ðàñòåíèÿ è æèâîòíûõ ëèøü äëÿ íàó÷íûõ öåëåé, íî èìïîðò òàêîé ïðîäóêöèè íå çàïðåùåí. ÃÌÎ-ïðîäóêòû ýòî ðåàëèè íàøèõ äíåé è áóäóùåå ÷åëîâå÷åñòâà, åñëè ìû íàó÷èìñÿ ïðàâèëüíî îöåíèâàòü è ìèíèìèçèðîâàòü ðèñêè ãåííîé èíæåíåðèè
×åëîâåê îêàçûâàë âëèÿíèå íà ãåíû ðàñòåíèé, êîãäà åùå íå èìåë ïîíÿòèÿ î ñàìîì èõ ñóùåñòâîâàíèè, îòáèðàÿ äëÿ âûðàùèâàíèÿ ñåìåíà îò ñàìûõ âêóñíûõ è óðîæàéíûõ îñîáåé.  ïîñëåäíèå äåñÿòèëåòèÿ ê ïðîñòîé ñåëåêöèè ïðèñîåäèíèëèñü ìåòîäû ãåííîé èíæåíåðèè. Ñðåäè ñîâðåìåííûõ ìåòîäîâ áîëüøèíñòâî ñâÿçàíî ñ âíåñåíèåì èçìåíåíèé íåïîñðåäñòâåííî â ñòðóêòóðó ÄÍÊ òàê ïîëó÷àþòñÿ ãåííî-ìîäèôèöèðîâàííûå ðàñòåíèÿ, íå âñòðå÷àþùèåñÿ â ïðèðîäå. Òàêèå ðàñòåíèÿ ìîãóò áûòü óñòîé÷èâû ê âðåäèòåëÿì, ýêñòðåìàëüíûì òåìïåðàòóðàì, îíè áûñòðåå ðàñòóò è ëó÷øå ïëîäîíîñÿò.
Îäíàêî íå òîëüêî îáûâàòåëè, íî è íåêîòîðûå ñïåöèàëèñòû îòíîñÿòñÿ ñ îïàñêîé ê ëþáûì ýêñïåðèìåíòàì, ñâÿçàííûì ñ íåïîñðåäñòâåííûì ðåäàêòèðîâàíèåì ãåíîâ, à ðåãóëèðóþùèå îðãàíû ââîäÿò íà íèõ æåñòêèå îãðàíè÷åíèÿ. Ïîýòîìó ó÷åíûå âûíóæäåíû ïðåäëàãàòü ìåòîäèêè, íå ïîäïàäàþùèå ïîä çàïðåòû è, ïðåäïîëîæèòåëüíî, ñ ìèíèìàëüíûìè ðèñêàìè.
Ñàìàÿ ïîïóëÿðíàÿ è ïðîäâèíóòàÿ ìåòîäèêà ñðåäè ñîâðåìåííûõ ñïîñîáîâ èçìåíåíèÿ ãåíîìà ðàñòåíèé âíåñåíèå â íåãî ãåíåòè÷åñêèõ êîíñòðóêöèé ñ ïîìîùüþ òåõíîëîãèè CRISPR-Cas9, êîòîðóþ ó÷åíûå «ïîäñìîòðåëè» ó áàêòåðèé. Îíà ïîçâîëÿåò ðàçðåçàòü ÄÍÊ â òî÷íî çàäàííûõ ó÷àñòêàõ è âñòðîèòü òóäà òðàíñãåí. Íî ïðè ïðèìåíåíèè ýòîé ìåòîäèêè âñå æå îñòàåòñÿ ðèñê íåñïåöèôè÷íîãî âîçäåéñòâèÿ íà ÄÍÊ.
Ìåíåå îïàñíûì è ïðàêòè÷åñêè íåèçâåñòíûì äëÿ øèðîêîé ïóáëèêè ÿâëÿåòñÿ öèñãåíåçèñ ââåäåíèå â ãåíîì ðàñòåíèÿ ãåíîâ îðãàíèçìîâ òîãî æå èëè áëèçêîãî âèäà, ñ êîòîðûìè îíî ìîæåò ñêðåùèâàòüñÿ â åñòåñòâåííûõ óñëîâèÿõ. Ïðîäîëæåíèåì ýòîé èäåè ÿâëÿåòñÿ èíòðàãåíåçèñ, êîãäà â ÄÍÊ ðàñòåíèÿ âñòðàèâàþò åãî ñîáñòâåííûé ãåí, ñîâìåùåííûé ñ ðåãóëÿòîðíûìè ó÷àñòêàìè äðóãèõ åãî ãåíîâ, ÷òî ïîçâîëÿåò ðåãóëèðîâàòü èõ àêòèâíîñòü.  ýòîì ñëó÷àå íàçâàòü òàêîå ðàñòåíèå ÃÌÎ ïðàêòè÷åñêè íåëüçÿ.
Ñóùåñòâóþò è ìåíåå èçâåñòíûå ìåòîäèêè, òàêèå êàê ñîìàòè÷åñêàÿ ãèáðèäèçàöèÿ èëè êîìáèíàöèè îáû÷íîãî ñêðåùèâàíèÿ èëè ïðèâèâîê ñ íîâåéøèìè ïîäõîäàìè. Íàïðèìåð, ýïèãåíåòè÷åñêèìè (íàäãåííûìè), ïðè êîòîðûõ ãåí ìîæíî çàñòàâèòü «çàìîë÷àòü» èëè, íàîáîðîò, «ðàçáóäèòü» ñ ïîìîùüþ ìåòèëèðîâàíèÿ ÄÍÊ.
À ìîæíî èñïîëüçîâàòü ãåíû, êîòîðûå íàçûâàþò «ïðûãàþùèìè» èëè òðàíñïîçîíàìè (ìîáèëüíûìè), ñïîñîáíûå ñàìîñòîÿòåëüíî ìåíÿòü ñâîå ïîëîæåíèå íà õðîìîñîìàõ. Îíè áûëè îòêðûòû â ñåðåäèíå ïðîøëîãî âåêà ó êóêóðóçû, à ñåé÷àñ îáíàðóæåíû ïðàêòè÷åñêè ó âñåõ èçâåñòíûõ âèäîâ æèâîòíûõ è ðàñòåíèé. Ñíà÷àëà òðàíñïîçîíû îòíîñèëè ê òàê íàçûâàåìîé ìóñîðíîé èëè áàëëàñòíîé ÄÍÊ.  îñíîâíîì îíè âåäóò ñåáÿ «òèõî», íî åñëè «ïðûãàþò», òî ìîãóò ïðèâîäèòü ê ìóòàöèÿì, ìåíÿÿ ñòðóêòóðó èëè ðåãóëÿöèþ ãåíîâ.
Ñåé÷àñ ìû çíàåì, ÷òî ìîáèëüíûå ýëåìåíòû îáåñïå÷èâàþò ïëàñòè÷íîñòü ðàñòèòåëüíîãî ãåíîìà, àäàïòèâíûé îòâåò íà ñòðåññîâûå óñëîâèÿ. Èññëåäîâàòåëè èç Êåìáðèäæñêîãî óíèâåðñèòåòà íà ïðèìåðå òîìàòîâ îáíàðóæèëè, ÷òî ñòðåññ â ðåçóëüòàòå îáåçâîæèâàíèÿ àêòèâèðóåò ðåòðîòðàíñïîçîíû ñåìåéñòâà Rider. Ýòè òðàíñïîçîíû, êàê áûëî èçâåñòíî, ÿâëÿþòñÿ îñíîâíûì èñòî÷íèêîì èçìåíåíèé îáëèêà ïëîäîâ òîìàòîâ, è îíè æå ïîìîãàþò ðàñòåíèÿì âûæèâàòü â çàñóõó.
Òðàíñïîçîíû ïðèðîäíûé èíñòðóìåíò, óæå ïðèñóòñòâóþùèé â ðàñòåíèè, íèêàêèå ÷óæåðîäíûå ãåíû ïðè ýòîì íå èñïîëüçóþòñÿ. È åñëè íàó÷èòüñÿ êîíòðîëèðóåìî àêòèâèðîâàòü «ïðûãàþùèå ãåíû», òî òàêèì ñïîñîáîì ìîæíî öåëåíàïðàâëåííî ïîëó÷àòü ðàñòåíèÿ ñ íîâûìè ïðèçíàêàìè. Òàêîé ïîäõîä ìîæåò çíà÷èòåëüíî ñîêðàòèòü âðåìÿ âûâåäåíèÿ ðàñòåíèé ñ íóæíûìè ñâîéñòâàìè, â äàííîì ñëó÷àå óñòîé÷èâûõ ê çàñóõå.
Ôîòî: https://pixabay.com
Источник
Традиционная селекция микроорганизмов (в основном бактерий и грибов) основана на экспериментальном мутагенезе и отборе наиболее продуктивных штаммов. Но и здесь есть свои особенности. Геном бактерий гаплоидный, любые мутации проявляются уже в первом поколении. Хотя вероятность естественного возникновения мутации у микроорганизмов такая же, как и у всех других организмов (1 мутация на 1 млн. особей по каждому гену), очень высокая интенсивность размножения дает возможность найти полезную мутацию по интересующему исследователя гену.
В результате искусственного мутагенеза и отбора была повышена продуктивность штаммов гриба пеницилла более чем в 1000 раз. Продукты микробиологической промышленности используются в хлебопечении, пивоварении, виноделии, приготовлении многих молочных продуктов. С помощью микробиологической промышленности получают антибиотики, аминокислоты, белки, гормоны, различные ферменты, витамины и многое другое.
Микроорганизмы используют для биологической очистки сточных вод, улучшений качеств почвы. В настоящее время разработаны методы получения марганца, меди, хрома при разработке отвалов старых рудников с помощью бактерий, где обычные методы добычи экономически невыгодны.
Биотехнология — использование живых организмов и их биологических процессов в производстве необходимых человеку веществ. Объектами биотехнологии являются бактерии, грибы, клетки растительных и животных тканей. Их выращивают на питательных средах в специальных биореакторах.
Новейшими методами селекции микроорганизмов, растений и животных являются клеточная, хромосомная и генная инженерия.
Генная инженерия
Генная инженерия — совокупность методик, позволяющих выделять нужный ген из генома одного организма и вводить его в геном другого организма. Растения и животные, в геном которых внедрены «чужие» гены, называются трансгенными, бактерии и грибы — трансформированными. Традиционным объектом генной инженерии является кишечная палочка, бактерия, живущая в кишечнике человека. Именно с ее помощью получают гормон роста — соматотропин, гормон инсулин, который раньше получали из поджелудочных желез коров и свиней, белок интерферон, помогающий справиться с вирусной инфекцией.
Процесс создания трансформированных бактерий включает в себя следующие этапы.
- Рестрикция — «вырезание» нужных генов. Проводится с помощью специальных «генетических ножниц», ферментов — рестриктаз.
- Создание вектора — специальной генетической конструкции, в составе которой намеченный ген будет внедрен в геном другой клетки. Основой для создания вектора являются плазмиды. Ген вшивают в плазмиду с помощью другой группы ферментов — лигаз. Вектор должен содержать все необходимое для управления работой этого гена — промотор, терминатор, ген-оператор и ген-регулятор, а также маркерные гены, которые придают клетке-реципиенту новые свойства, позволяющие отличить эту клетку от исходных клеток.
- Трансформация — внедрение вектора в бактерию.
- Скрининг — отбор тех бактерий, в которых внедренные гены успешно работают.
- Клонирование трансформированных бактерий.

Образование рекомбинантных плазмид:
1 — клетка с исходной плазмидой; 2 — выделенная плазмида; 3 — создание вектора; 4 — рекомбинантная плазмида (вектор); 5 — клетка с рекомбинантной плазмидой.
Эукариотические гены, в отличие от прокариотических, имеют мозаичное строение (экзоны, интроны). В бактериальных клетках отсутствует процессинг, а трансляция во времени и пространстве не отделена от транскрипции. В связи с этим для пересадки эффективнее использовать искусственно синтезированные гены. Матрицей для такого синтеза является иРНК. С помощью фермента обратная транскриптаза на этой иРНК сперва синтезируется цепь ДНК. Затем на ней с помощью ДНК-полимеразы достраивается вторая цепь.
Хромосомная инженерия
Хромосомная инженерия — совокупность методик, позволяющих осуществлять манипуляции с хромосомами. Одна группа методов основана на введении в генотип растительного организма пары чужих гомологичных хромосом, контролирующих развитие нужных признаков (дополненные линии), или замещении одной пары гомологичных хромосом на другую (замещенные линии). В полученных таким образом замещенных и дополненных линиях собираются признаки, приближающие растения к «идеальному сорту».
Метод гаплоидов основан на выращивании гаплоидных растений с последующим удвоением хромосом. Например, из пыльцевых зерен кукурузы выращивают гаплоидные растения, содержащие 10 хромосом (n = 10), затем хромосомы удваивают и получают диплоидные (n = 20), полностью гомозиготные растения всего за 2–3 года вместо 6–8-летнего инбридинга.
Сюда же можно отнести и метод получения полиплоидных растений (см. Лекция 23 «Селекция растений»).
Клеточная инженерия
Клеточная инженерия — конструирование клеток нового типа на основе их культивирования, гибридизации и реконструкции.
Клетки растений и животных, помещенные в питательные среды, содержащие все необходимые для жизнедеятельности вещества, способны делиться, образуя клеточные культуры. Клетки растений обладают еще и свойством тотипотентности, то есть при определенных условиях они способны сформировать полноценное растение. Следовательно, можно размножать растения в пробирках, помещая клетки в определенные питательные среды. Это особенно актуально в отношении редких или ценных растений.
С помощью клеточных культур можно получать ценные биологически активные вещества (культура клеток женьшеня). Получение и изучение гибридных клеток позволяет решить многие вопросы теоретической биологии (механизмы клеточной дифференцировки, клеточного размножения и др.). Клетки, полученные в результате слияния протопластов соматических клеток, относящихся к разным видам (картофеля и томата, яблони и вишни и др.), являются основой для создания новых форм растений. В биотехнологии для получения моноклональных антител используются гибридомы — гибрид лимфоцитов с раковыми клетками. Гибридомы нарабатывают антитела, как лимфоциты, и обладают возможностью неограниченного размножения в культуре, как раковые клетки.
Метод пересадки ядер соматических клеток в яйцеклетки позволяет получить генетическую копию животного, то есть делает возможным клонирование животных. В настоящее время получены клонированные лягушки, получены первые результаты клонирования млекопитающих.
Метод слияния эмбрионов на ранних стадиях делает возможным создание химерных животных. Таким способом были получены химерные мыши (слияние эмбрионов белых и черных мышей), химерное животное овца-коза.
Перейти к лекции №24 «Селекция животных»
Смотреть оглавление (лекции №1-25)
Похожие материалы:
►Генная инженерия: ее развитие и методы
►Селекция и генная инженерия. Трансгенные растения
Источник
