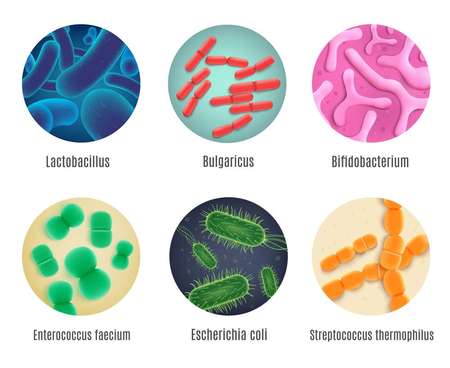
Микроорганизмы желудочно кишечного тракта человека
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 25 июня 2020; проверки требуют 48 правок.
Микрофлора кишечника — микроорганизмы, которые живут в желудочно-кишечном тракте в симбиозе с носителем.
Кишечник человека содержит в среднем около 50 триллионов микроорганизмов, что примерно в 1,3 раза больше, чем суммарное количество клеток в организме[1][2]. Бактерии составляют подавляющее большинство микрофлоры в прямой кишке[3] и до 60 % сухой массы фекалий[4]. Где-то между 300[5] и 1000[6] различных видов живут в кишечнике, по большинству оценок порядка 500[7][8]. Однако, вероятно, что 99 % бактерий относятся к 30—40 видам[9]. Дрожжи также составляют часть микрофлоры кишечника, но об их активности известно мало.
Значение для организма[править | править код]
Исследования показывают, что отношения между кишечником и микрофлорой не являются просто комменсализмом (то есть безвредным сосуществованием), но скорее формой мутуализма, то есть взаимовыгодными отношениями[6]. Хотя люди могут выжить и без микрофлоры кишечника[7], микроорганизмы выполняют для хозяина ряд полезных функций, например , анаэробное пищеварение неиспользованного материала для обеспечения себя энергией, тренировка иммунной системы и предотвращение роста вредных видов[4]. Однако микрофлора кишечника не всегда исключительно полезна: считается, что некоторые микроорганизмы в определённых случаях могут вызывать болезни. Также она способна производить биотрансформацию лекарственных препаратов и оказывать воздействие на экспрессию генов человека, регулирующих метаболизм, вызывая нежелательные побочные эффекты[10].
В норме чрезмерному росту бактерий в тонкой кишке препятствуют:
- нормальная секреция соляной кислоты (предупреждает размножение бактерий в верхних отделах желудочно-кишечного тракта);
- илеоцекальный клапан (предупреждает поступление бактерий из толстой кишки в тонкую);
- нормальная толкательная моторика тонкой кишки (предупреждает застой кишечного содержимого).
Бифидо- и лактобактерии имеют выраженную антагонистическую активность в отношении патогенных бактерий и регулируют количественный и качественный состав кишечной микрофлоры в норме, задерживают рост и размножение в нём патогенных и условно-патогенных микробов.
Кишечные сапрофиты, по сравнению с патогенными бактериями, содержат большое количество ферментов, размножаются более активно, поэтому легче утилизируют питательные вещества и кислород. Они производят разнообразные бактерицидные и бактериостатические вещества, в том числе антибиотикоподобные.
Микроорганизмы[править | править код]
Виды микроорганизмов в кишечнике :
- анаэробы
- бактероиды
- бифидобактерии
- энтерококки
- клостридии
- эубактерии
- аэробы
- энтеробактерии
- стрептококки
- стафилококки
- лактобактерии
- грибы (которые бактериями, разумеется, не являются)
В желудке в норме за счёт кислой среды количество микробов незначительно (лактобациллы, стрептококки, сарцины). Двенадцатиперстная кишка и проксимальный отдел тонкой кишки у здоровых людей стерильные за счёт наличия в них агрессивных пищеварительных ферментов. В дистальной части тонкой кишки в 1 мл содержимого насчитывается 107−108 микробов, в равном количестве аэробных и анаэробных. В 1 мл содержимого дистального отдела толстой кишки находится 109−1012 микробов около 400 видов. Наибольшая плотность обсемененности наблюдается в прямой кишке. Микрофауна кала является фактически микрофауной дистального отдела толстой кишки.
В норме более 95 % микрофлоры кала составляют анаэробы: лактобациллы, бифидобактерии и бактероиды. Аэробная микрофлора представлена (по частоте выделения и количества) кишечной палочкой, энтерококком. Реже в незначительном количестве обнаруживают стафилококки, стрептококки, клебсиеллы, протей, клостридии, дрожжеподобные грибы.
Все микроорганизмы, которые в норме заселяют толстую кишку, делят на три группы:
- основную (лактобактерии, бифидобактерии и бактероиды),
- сопутствующую (штаммы кишечной палочки, энтерококки)
- окончательную (стафилококки, грибы, протей).
См. также[править | править код]
- Микрофлора человека
Примечания[править | править код]
- ↑ Ученые: бактерий в теле человека не в 10 раз больше, чем своих клеток | РИА Новости
- ↑ Ron Sender, Shai Fuchs, Ron Milo. Revised Estimates for the Number of Human and Bacteria Cells in the Body // PLOS Biology. — 2016-08-19. — Т. 14, вып. 8. — С. e1002533. — ISSN 1545-7885. — doi:10.1371/journal.pbio.1002533.
- ↑ Sandra Macfarlane, Elizabeth Furrie, John H. Cummings, George T. Macfarlane. Chemotaxonomic Analysis of Bacterial Populations Colonizing the Rectal Mucosa in Patients with Ulcerative Colitis // Clinical Infectious Diseases. — 2004-06-15. — Т. 38, вып. 12. — С. 1690—1699. — ISSN 1058-4838. — doi:10.1086/420823.
- ↑ 1 2 Alison M. Stephen, J. H. Cummings. THE MICROBIAL CONTRIBUTION TO HUMAN FAECAL MASS (англ.) // Journal of Medical Microbiology (англ.)русск.. — Microbiology Society (англ.)русск., 1980. — Vol. 13, iss. 1. — P. 45—56. — doi:10.1099/00222615-13-1-45.
- ↑ Guarner F and Malagelada JR. 2003. Gut flora in health and disease. The Lancet, Volume 361, Issue 9356, 8 February 2003, Pages 512—519. PMID 12583961. Accessed September 15, 2007
- ↑ 1 2 A dynamic partnership: Celebrating our gut flora. Cynthia L.Sears. Anaerobe. Volume 11, Issue 5, October 2005, Pages 247—251. doi.org/10.1016/j.anaerobe.2005.05.001
- ↑ 1 2 Who controls the crowd? New findings and old questions about the intestinal microflora. Ulrich Steinhoff. — Immunology Letters. Volume 99, Issue 1, 15 June 2005, Pages 12-16 doi.org/10.1016/j.imlet.2004.12.013
- ↑ Gibson RG. 2004. Fibre and effects on probiotics (the prebiotic concept). Clinical Nutrition Supplements, Volume 1, Issue 2, Pages 25-31.
- ↑ Beaugerie L and Petit JC. 2004. Antibiotic-associated diarrhoea. Best Practice & Research Clinical Gastroenterology, Volume 18, Issue 2, Pages 337—352
- ↑ Анна Кузнецова. Микробные фармацевты внутри нас (рус.) // Наука и жизнь. — 2020. — № 2. — С. 44—49.
- ↑ Kenneth Todar. The Normal Bacterial Flora of Humans. Todar’s Online Textbook of Bacteriology (2012). Дата обращения: 25 июня 2016.
Источник
В желудочно–кишечном тракте человека встречается облигатная (главная микрофлора), факультативная (условно-патогенная и сапрофитная микрофлора) и транзиторная микрофлора (случайно попавшие в ЖКТ микроорганизмы).
В пищеводе и желудке обычно определяется транзиторная микрофлора, попадающая в них с пищей или из ротовой полости.
Несмотря на попадание в желудок большого количества микробов, у здоровых людей в норме в желудке определяется небольшое количество микроорганизмов (менее 103 КОЕ/мл). Это связано с кислым значением рН содержимого желудка и бактерицидными свойствами желудочного сока, который надежно защищает человека от проникновения в кишечник патогенных и условно-патогенных бактерий.
В желудочном соке встречаются в основном кислотоустойчивые бактерии–лактобактерии, дрожжевые грибы. У некоторых людей в нем определяются стрептококки, S. ventriculus, B. subtilis, анаэробные грамположительные кокки.
В толще слизистой оболочки желудка обнаруживаются анаэробы вейлонеллы, бактероиды, пептококки.
При исследовании здоровых детей в возрасте 8–15 лет в слизистой антральной части желудка были выявлены стафилококки, стрептококки, энтерококки, коринебактерии, пептококки, лактобактерии и пропионибактерии. Микробиологическое исследование содержимого желудка проводят сравнительно редко.
Количество и состав микробов в тонком кишечнике меняется в зависимости от отдела кишечника.
Общее количество микробов в тонком кишечнике составляет не более 104–105 КОЕ/мл содержимого. Низкая концентрация микробов обусловлена действием желчи, наличием ферментов поджелудочной железы, кишечной перистальтики, обеспечивающей быстрое удаление микробов в дистальный отдел кишечника; выработкой иммуноглобулинов клетками слизистой оболочки, состоянием кишечного эпителия и слизи, выделяемой бокаловидными клетками кишечника, содержащими ингибиторы роста микробов.
Микрофлора тонкого кишечника представлена преимущественно грамположительными факультативно–анаэробными и анаэробными бактериями (энтерококками, лактобактериями, бифидобактериями), дрожжеподобными грибами, реже встречаются бактероиды и вейлонеллы, крайне редко энтеробактерии.
После приема пищи количество микробов в тонком кишечнике может значительно увеличится, но затем в короткие сроки оно быстро возвращается к исходному уровню. В нижних отделах тонкого кишечника (в подвздошной кишке) количество микробов увеличивается и может достигать 107 КОЕ/мл содержимого.
В толстом кишечнике грамположительная флора меняется на грамотрицательную. Количество облигатных анаэробов начинает превышать число факультативных анаэробов. Появляются представители микробов, характерные для толстого кишечника.
Росту и развитию микробов в толстом кишечнике способствуют отсутствие пищеварительных ферментов, наличие большого количества питательных веществ, длительное нахождение пищи, особенности строения слизистой оболочки и, в частности, слизистые наложения толстого кишечника. Они обуславливают органный тропизм некоторых видов анаэробных бактерий, образующих в результате своей жизнедеятельности продукты, используемые факультативно-анаэробной флорой, которые в свою очередь создают условия для жизни облигатных анаэробов.
В толстом кишечнике человека присутствуют более 400 видов различных микробов, причем число анаэробов в 100–1000 раз превышает число факультативных анаэробов. Облигатные анаэробы составляют 90-95% всего состава. Они представлены бифидобактериями, лактобактериями, бактероидами, вейлонеллами, пептострептококками, клостридиями и фузобактериями.
На долю других микроорганизмов приходится 0,1– 0,01% это остаточная микрофлора: энтеробактерии (протеи, клебсиеллы, серрации), энтерококки, стафилококки, стрептококки, бациллы, дрожжевые грибы (рис.3). В кишечнике могут жить условно-патогенные амебы, трихомонады, некоторые виды кишечных вирусов.
В толстом кишечнике человека выделяют М-мукозную микрофлору – микробы, обитающие в толще слизистой оболочки. Количество микробов в толще слизистой составляет 108 КОЕ на грамм ткани кишечника. Некоторые авторы называют мукозную микрофлору – «бактериальный дерн».
Микробы, живущие в просвете кишечника человека называют П–микрофлора (просветная или полостная). Количество микробов в фекалиях человека достигает 1012 КОЕ/г. содержимого и составляет 1/3 часть фекальных масс человека. На долю факультативных анаэробов приходится 5-10% микрофлоры толстого кишечника. В состав ее входят: кишечная палочка и энтерококки.
Облигатная постоянная микрофлора кишечника человека представлена, в основном, бифидобактериями, лактобактериями, кишечными палочками и энтерококками. Факультативная флора встречается реже, она представлена другими анаэробными и факультативно – анаэробными бактериями.
Дисбактериоз (дисбиоз, дисмикробиоценоз) кишечника – качественные и количественные изменения микрофлоры. Дисбактериоз сопровождается снижением облигатной анаэробной флоры (бифидо- и лактобактерии) и увеличением условно – патогенной микрофлоры, которые в норме отсутствуют или встречаются в небольшом количестве (стафилококки, псевдомонады, дрожжеподобные грибы, протеи и т. д.). Появление дисбактериоза может привести к иммунологическим нарушениям с возможным развитием желудочно-кишечных расстройств.
Развитию дисбактериоза у человека способствуют экзогенные и эндогенные факторы: инфекционные заболевания органов пищеварения, заболевания ЖКТ, печени, онкологическая патология, аллергические заболевания.
Изменению микрофлоры способствует прием антибиотиков, гормонов, иммунодепрессантов, цитостатиков, психотропных, слабительных и противозачаточных препаратов, воздействие на организм промышленных ядов и пестицидов. Большое влияние на состав микрофлоры оказывают сезон года, питание человека, стрессы, курение, наркомания, алкоголизм.
Появление дисбактериоза у новорожденных может быть обусловлено бактериальным вагинозом и маститом у матери, проведением реанимационных мероприятий, поздним прикладыванием к груди, длительным пребыванием в родильном доме, незрелостью моторной функции кишечника, непереносимостью грудного молока, синдромом мальадсорбции.
В грудном возрасте развитию дисбактериоза способствуют: раннее искусственное вскармливание, частые ОРВИ, рахит, анемии, гипотрофии, аллергические и психоневрологические заболевания.
Возрастные изменения микрофлоры кишечника у детей
При внутриутробном развитии плод стерилен, поскольку он защищен оболочкой непроницаемой для микроорганизмов. Однако, после разрыва плодной оболочки и при прохождении плода по родовым путям, микроорганизмы начинают заселять сначала кожу ребенка, а в дальнейшим попадают и в желудочно-кишечный тракт.
В течение первого дня жизни кишечный тракт ребенка заселяется случайной кокковой флорой, попавшей в него из окружающей среды, с рук персонала родильного дома и с грудных желез матери. К 7 – 9 дню у детей, находящихся на грудном вскармливании, кокковая флора заменяется на бифидобактерии, так как в женском молоке находится биогенный, термостабильный фактор, который способствует быстрому заселению ЖКТ этими бактериями.
Количество бифидобактерий на 1г фекалий достигает 109 – 110 микробных клеток (82-95% кишечной микрофлоры), прочие бактерии представлены лактобактериями, кишечными палочками, энтерококками, стафилококками.
У недоношенных детей и детей, находящихся на искусственном вскармливании, бифидофлора появляется позднее и количество этих бактерий в их кишечнике находится в почти равном соотношении с лактобактериями, кишечными палочками, другими энтеробактериями, энтерококками, стафилококками и клостридиями.
При переводе детей на смешанное вскармливание и добавлении коровьего молока в кишечнике появляются грамотрицательные анаэробы (бактероиды), увеличивается число энтеробактерий и кокков.
Этапы формирования микрофлоры кишечника
Становление нормального микробиоценоза имеет возрастные особенности. У новорожденного ЖКТ в течение 10–20 суток стерилен (асептическая фаза). Первичная микробная контаминация осуществляется за счет флоры влагалища матери, основу которой составляют лактобациллы. В первые 2 – 4 дня жизни (фаза «транзиторного» дисбактериоза) происходит заселение кишечника ребенка микробами. Это зависит от следующих факторов:
– состояния здоровья матери, в частности, микробиоценоза ее родовых путей;
– характера питания ребенка, при этом несомненный приоритет принадлежит грудному вскармливанию;
– особенностей микробного загрязнения окружающей среды;
– активности генетически детерминированных неспецифических защитных механизмов (активности макрофагов, секреции лизоцима, пероксидазы, нуклеаз и.т.д);
– наличия и степени активности пассивного иммунитета, передаваемого матерью через кровь трансплацентарно и с молоком при первом кормлении грудью.
В течение последующих 2–3 дней жизни (фаза трансплантации) состав микроорганизмов подвержен значительным колебаниям. Относительная стабилизация микрофлоры наблюдается к концу первого месяца жизни. Бифидофлора становится доминирующей, вследствие утилизации бифидогенных факторов, содержащихся в грудном молоке.
Искусственное и смешанное вскармливание задерживает по времени фазу трансплантации. У таких детей бифидофлора существенно угнетена, в этом их кардинальное отличие от детей, находящихся на естественном вскармливании.
К 4 – 7 годам происходит возрастное становление микробиоценоза – количество бифидобактерий уменьшается до 10-8 КОЕ/г, изменяется видовой состав (исчезают B. infantis, появляются B. adolescentis, уменьшается количество B. bifidum), возрастает численность грамположительных аспорогенных микроорганизмов, уменьшается содержание лактобактерий до 10-6 КОЕ/г.
Факторы грудного молока, влияющие на заселение микрофлоры
Еще в 1981г. Hansson показал, что дети, рожденные путем кесарева сечения, имеют значительно более низкое содержание лактобактерий, чем появившиеся естественным путем.
Roberfroid в 2000г. окончательно доказал, что только у детей, находящихся на естественном вскармливании (грудное молоко), в микрофлоре кишечника преобладают бифидобактерии, с чем и связал меньший риск развития гастроинтестинальных инфекционных заболеваний. Самое главное чтоб, прежде всего, бифидобактерии попали в толстый кишечник ребенка, а там при употреблении женского молока, содержащего бифидоактивные олигосахариды, происходит быстрая колонизация бифидобактерий.
При искусственном вскармливании различными молочными смесями, даже если ребенку вводят бифидобактерии, нарушается микробная колонизация кишечника, т.к. во многих смесях не содержатся бифидоактивные олигосахариды, а это приводит к формированию анормальной микрофлоры, в которой преобладают условно-патогенные микроорганизмы.
Прием бифидоактивных олигосахаридов в виде отваров круп, а так же прием донорского грудного молока стимулирует рост бифидобактерий у ребенка.
У естественно вскармливаемых детей доминирует L. bifidus, прочие бактерии представлены кишечными палочками, энтерококками и стафилококками. Создаются благоприятные условия преимущественно для роста бифидобактерий (B. bifidum B. infantis и B. breve). Кроме того, основным видом энтеробактерий являются E. coli).
MacNelly в монографии 1999г. приводит данные, что состав кишечной флоры ребенка после 2 лет практически не отличается от взрослого: более 400 видов бактерий, причем большинство из которых анаэробы, плохо поддающихся культивированию.
Микрофлора кишечника в пожилом и старческом возрасте
Процесс старения приводит к изменению практически всех слоев стенок желудка. Изменяется слизистая оболочка. Уменьшается количество мышечных волокон и секреторных клеток. Частично нарушается иннервация желудочно-кишечного тракта.
Общая длина кишечника с возрастом увеличивается, чаще происходит удлинение отдельных участков толстой кишки. В стенках кишечника происходит атрофические изменения, приводящие к изменению мембранного пищеварения. В результате нарушается всасывание белков, жиров и углеводов.
Так же меняется и микрофлора: увеличивается количество бактерий гнилостной группы, уменьшается количество молочнокислых микроорганизмов. Это способствует увеличению выделяемых микробами эндотоксинов, в результате чего нарушается функциональная деятельность кишечника.
Формируется синдром избыточного бактериального роста в тонкой кишке, который характеризуется мальдигестией и мальабсорбцией. Ведущим клиническим симптомом оказываются запоры, боли в животе, метеоризм, тошнота, отрыжка, тенезмы, снижение аппетита, неприятные ощущения во рту.
Источник
Относительно недавно в медицинских кругах сложилось утверждение, что человеческим организмом, эмоциями, настроением, здоровьем и поступками правят…бактерии! Место обитания которых – кишечник. Публика мгновенно разделилась на 2 лагеря. Одни утверждают, что бактерии действительно обладают способностью управлять нами, и обосновывают мнение фактами, другие признают это полным антинаучным бредом и, как ни парадоксально, тоже приводят аргументы. Попробуем разобраться и понять, что такое микрофлора, зачем она нужна, как бактерии управляют нами, за что их называют вторым мозгом, и как помочь бактериям сделать управление эффективным.
Что такое микрофлора кишечника
Флора кишечника – это то, что человек получает с момента рождения и развивает на протяжении первых 7-10 лет. Со временем набор микроорганизмов становится разнообразнее и состоит из лактобактерий, бифидобактерий, грибков и кишечных палочек. Все они живут в дружном соседстве не только между собой, но и с патогенной микрофлорой, не позволяя ей размножаться и причинять организму вред.
Считается, что патогенная микрофлора составляет не более 15% от общей массы бактерий. А всего ученые умы насчитывают около 100 триллионов простейших микроорганизмов в нашем кишечнике, вес которых составляет в среднем 1,5 килограмма.
В норме, питанием и образом жизни человек способен длительно поддерживать удачный симбиоз своих поселенцев. Понимание этого процесса поможет значительно повысить качество жизни и здоровья.
За что отвечает микрофлора кишечника
Пищеварение
Одна из важнейших функций кишечных бактерий – участие в процессе переваривания пищи. Это такой гигантский завод по очистке зёрен от плевел. Когда вся поступающая пища, белки, жиры и углеводы расщепляются под воздействием ферментов, работу которых активизирует кишечник. Кишечник – финальная, но самая трудоемкая и времезатратная часть процесса пищеварения. Именно там с помощью микробиома запускается процесс сортировки полезных веществ от ненужного мусора. От того насколько здоров кишечник и весь пищеварительный тракт, зависит и качество сортировки пищи, и количество полезных веществ, которые всасываются и усваиваются именно в кишечнике.
Защита
Один в поле не воин – фраза, которая удачно характеризует работу кишечника. Чем меньше в нём “хороших” бактерий, тем больше места достается “плохим”. Полезные бактерии в процессе жизнедеятельности подавляют рост возбудителей инфекционных заболеваний, поддерживая тем самым защитные функции всего организма.
Иммунитет
Когда защита организма сильна, болезнь не пройдет. И большую роль в этом играет иммунитет, родина которого – кишечник. Как это происходит? Кишечные бактерии стимулируют синтез иммуноглобулинов – особых белков, повышающих защитные силы организма в отношении опасных инфекций. Иммуноглобулины населяют стенки кишечника, при достаточном количестве которых патогенные микроорганизмы не проникают. Также полезные бактерии содействуют созреванию системы фагоцитирующих клеток (неспецифический иммунитет), способных к поглощению и уничтожению патогенных микробов.
Синтез витаминов
Дружественные бактерии, живущие в кишечнике жизненно необходимы человеку для синтеза, хранения и поставки витаминов в организм:
- Витамин В-12
- Фолиевая кислота / Витамин В-9
- Витамин К
- Рибофлавин / Витамин В-2
- Биотин / Витамин В-7
- Никотиновая кислота / Витамин В-3
- Пантотеновая кислота / Витамин В-5
- Пиридоксин / Витамин В-6
- Тиамин / Витамин В-1
Среди них такие, которые нигде больше в организме не вырабатываются. Эта миссия возложена на бактерии. Витамины группы В жизненно необходимы человеку. Они содержат в порядке нервную систему, участвуют в обменных процессах, помогают противостоять стрессам и депрессии. Если нарушена микрофлора, синтез витаминов не происходит должным образом и неприятных последствий не избежать. Кроме того, никакие курсы витаминов не помогут. Вы не ощутите положительный эффект просто потому, что они не будут всасываться в кишечнике.
Как кишечная микрофлора помогает похудеть
Ещё один центр внимания ученых и исследователей – это зависимость веса человека от разнообразия микрофлоры. Так, недавние исследования американских ученых подтвердило этот факт. В ходе эксперимента наборы кишечных бактерий от людей-близнецов поместили в кишечник стерильных мышей. В одном наборе люди-близнецы были худые, в другом страдали ожирением. Микробы, взятые у худых близнецов вызывали похудение у мышей, а бактерии от полных близнецов вызывали у мышей ожирение. Но через время, когда мышей сажали в одну клетку, мыши с ожирением начинали стремительно терять вес.
Ученые сделали предположение, что микрофлора способна управлять пищевыми привычками, требуя от человека тех или иных продуктов, которые будут способствовать росту либо патогенных, либо “худых” бактерий. Лучшим рационом для некоторых бактерий являются жиры и они требуют их постоянно снова и снова, другим жизненно необходим сахар. Именно на зависимости пищевых потребностей и разнообразием бактерий в кишечнике, ученые выдвинули теорию, что кишечные поселенцы, стремятся брать верх над человеком и манипулировать химическим составом среды обитания ради собственных целей и выгоды. Это, в свою очередь, может означать манипуляции нашим поведением (нервничаем, если не едим сладкое, )путем воздействия с помощью нервных импульсов на центры голода, желание съесть тот или иной продукт, к тем или иным продуктам питания, или чувству отвращения от некоторых продуктов.
Почему нарушается баланс микрофлоры
Этот баланс очень хрупок и легко подвержен внешнему влиянию. И происходит это по нескольким причинам:
- прием антибиотиков
- нарушение режима питания
- злоупотребление сахаром и алкоголем
- отравления
- приём некоторых гормональных препаратов
- заболевания пищеварительной системы
- стресс
- приём некоторых лекарств – нестероидных противовоспалительных средств.
Признаки нарушения микрофлоры
- Нарушение стула – запоры, диарея, нерегулярный стул, вздутие, колики, боль
- Нарушения работы ЖКТ – появление тяжести, изжога, отрыжка, увеличение массы тела.
- Обезвоживание – появление ломкости и сухости волос и ногтей, кожных покровов,
- Интоксикация организма – тошнота, болезненный цвет лица, прыщи и угревая сыпь.
- Наличие неприятного запаха при дыхании, неприятный запах фекалий
- Изменения нервной системы – быстрая утомляемость, сонливость, отсутствие настроения, снижение работоспособности.
- Головокружения и головные боли
Как восстановить микрофлору кишечника
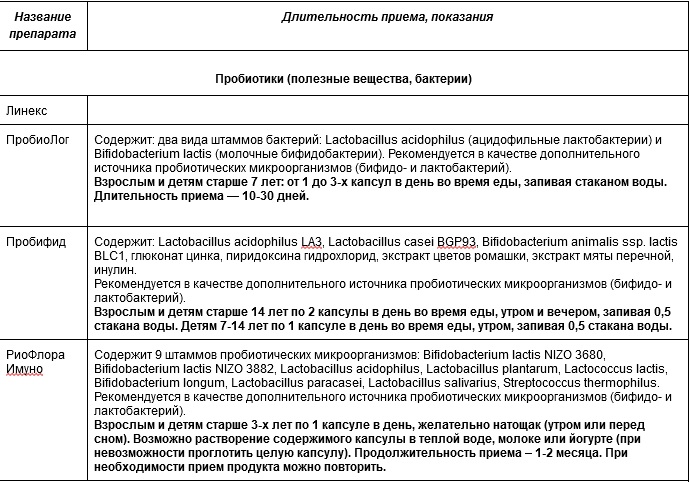
Процесс восстановления микрофлоры не быстрый. Важно не только скорректировать режим питания, но и активно помогать организму “наращивать” микробиом – правильно подобрать нужный препарат, содержащий пре- и пробиотики.
Линекс
Пробиолог
Пробифид


Бонус: могут ли микробы управлять человеческим поведением
Эта гипотеза сейчас становится очень популярной и, действительно, имеет на то ряд прямых и косвенных оснований. Кишечник называют вторым мозгом человека и бактерии, живущие в нем, действительно способны управлять человеком на уровне нервной системы.
В настоящий момент человечеству известно про наш организм многое, но не всё. Исследования в области микрофлоры кишечника и её влиянии на здоровье и качество организма находятся на зачаточной стадии, но привлекает всё больше внимания учёного мира. Так в ходе изучения микробиома человека подтвердилось существование сильной взаимосвязи между состоянием бактерий и работой иммунной, нервной и эндокринной систем. Некоторые ученые полагают, что бактерии могут выделять определенные сигнальные молекулы, влияющие на активность десятичного черепного нерва, проходящего от кишечника к головному мозгу, либо в данном процессе может быть задействован блуждающий нерв.
Сколько времени займет полное познание человека сказать невозможно, но можно быть уверенным, что мы подошли к чрезвычайно важным открытиям, которые, в будущем, решат множество проблем со здоровьем, помогут найти ключ к неизлечимым заболеваниям и тотально изменят привычную жизнь.
Будьте здоровы!
Источник